
Divercity recrute !
Contexte : le dispositif Divercity
Depuis l’adoption en 2005 de la Loi pour l’égalité des droits et des chances, la participation et la citoyenneté des personnes handicapées, les établissements recevant du public (commerces, etc.) doivent être accessibles. Si des aménagements existent, ils ciblent encore majoritairement les handicaps visibles, en particulier les difficultés motrices (rampes, sanitaires adaptés, etc.). Or, 80% des handicaps ne se voient pas. Les troubles du neurodéveloppement (TND), qui concernent une personne sur six, font le plus souvent partie de ces handicaps.
Pour répondre à ces besoins, le Centre iMIND présente Divercity, un réseau de lieux adaptés aux personnes avec TND. Ces lieux ont été sensibilisés grâce à une série de capsules vidéo présentant les difficultés rencontrées par ce public. En mettant en place des aménagements simples et peu coûteux, les établissements recevant du public peuvent adapter leur accueil afin de favoriser l’inclusion des personnes avec TND.
Dans quelques semaines, une application mobile répertoriera les lieux ayant rejoint Divercity. Elle permettra aux personnes qui le souhaitent de repérer ces lieux plus facilement.

Déploiement sur le territoire
Afin que de nouveaux établissements rejoignent le réseau Divercity, une seconde phase de démarchage va débuter !
Pour ces deux offres, tu bénéficieras d’une formation dédiée au TND et à Divercity.
Postes à pourvoir : ambassadeur·rice·s Divercity
Profil recherché :
- Être majeur·e
- Aisance relationnelle et goût du contact : tu aimes aller vers les autres et échanger.
- Capacité à sensibiliser et à convaincre : tu sais adapter ton discours à tes interlocuteur·rice·s.
- Autonomie et esprit d’initiative
- Sensible aux questions d’inclusion
- Une connaissance des troubles du neurodéveloppement serait un plus, mais n’est pas indispensable
En binôme, tu seras chargé·e de :
- Aller à la rencontre des établissements recevant du public (commerces, restaurants, lieux culturels, etc.) pour les sensibiliser à l’accueil des personnes avec des TND.
- Présenter le projet Divercity et expliquer les bénéfices d’une meilleure accessibilité.
- Accompagner les établissements dans leurs premières démarches pour intégrer le réseau Divercity.
Points clés du poste d’ambassadeur·rice Divercity :
- Contrat : CDD de 3 mois à temps partiel (14h/mois)
- Durée hebdomadaire : 3h30/semaine
- Lieu : centre-ville de Lyon
- Rémunération : 148,78 € brut par mois
Le détail complet de l’offre se trouve sur la fiche de poste.
Pour candidater, envoie ton CV, une lettre de motivation et tes créneaux disponibles pour le poste (du lundi au vendredi entre 10h et 17h, plages de 3h30 minimum) à l’adresse suivante d’ici le 22 février 2026, en précisant dans l’objet « Candidature Ambassadeur·rice Divercity » : contact@divercity.app.
Poste à pourvoir : chargé·e de mission – relation avec les établissements
Profil recherché :
- Être majeur·e
- Aisance relationnelle et goût du contact : tu aimes aller vers les autres et échanger.
- Capacité à sensibiliser et à convaincre : tu sais adapter ton discours à tes interlocuteur·rice·s.
- Aisance rédactionnelle
- Autonomie et esprit d’initiative
- Sensible aux questions d’inclusion
- Une connaissance des troubles du neurodéveloppement serait un plus, mais n’est pas indispensable
En lien avec les ambassadeur·rice·s déployé·e·s sur le territoire et l’équipe d’iMIND, tu seras chargé·e de :
- Rechercher le bon interlocuteur au sein des établissements ainsi que ses coordonnées
- Contacter les responsables d’établissement par mail et/ou téléphone pour leur présenter Divercity
- Prendre des rendez-vous pour les ambassadeur·rice·s
- Présenter Divercity et expliquer les bénéfices d’une meilleure accessibilité (téléphone, mail, visio)
- Accompagner les établissements dans leurs premières démarches pour intégrer le réseau Divercity.
Points clés du poste de chargé·e de mission Divercity :
- Contrat : CDD de 3 mois à temps partiel (14h/mois)
- Durée hebdomadaire : 3h30/semaine
- Lieu : Campus hospitalier Le Vinatier (Bron)
- Télétravail possible après la phase de montée en autonomie
- Rémunération : 148,78 € brut par mois
Le détail complet de l’offre se trouve sur la fiche de poste.
Pour candidater, envoie ton CV, une lettre de motivation et tes créneaux disponibles pour le poste (du lundi au vendredi entre 10h et 17h, plages de 3h30 minimum) à l’adresse suivante d’ici le 22 février 2026, en précisant dans l’objet « Candidature Chargé·e de mission Divercity » : contact@divercity.app.
Recherche
Divercity est un dispositif innovant. C’est la première fois que des aménagements de ce type sont mis en place en conditions réelles. À ce titre, des projets de recherche ont vu le jour afin de valider la pertinence du dispositif et son impact sur la qualité de vie des populations concernées.
Une première étude (confiée au cabinet de design sociétal Mengrov) vise à évaluer les comportements des commerçants suite à la sensibilisation effectuée par les capsules vidéo.
Une deuxième étude (menée par l’Université Lumière Lyon 2) servira à vérifier l’acceptabilité des aménagements par les commerçants. Elle mettra en lumière les obstacles rencontrés par les commerçants, l’objectif étant de lever ces problèmes.
Enfin, trois études complémentaires (conduites par iMIND, le Vinatier et l’Institut des sciences cognitives Marc Jeannerod) serviront à analyser les effets de Divercity dans un environnement urbain réel.
Poste à pourvoir : un·e post-doctorant·e en Sciences humaines et sociales, dont sociologie et psychologie (iMIND, Le Vinatier, ISC Marc Jeannerod)
Nous recherchons un·e post-doctorant·e afin d’évaluer le dispositif dans un environnement urbain réel au travers de trois études complémentaires :
- Étude 4a : Analyse des données d’usage générées par l’application
- Étude 4b : Évaluation en situation écologique de l’adéquation des aménagements aux besoins individuels
- Étude 4c : Étude longitudinale de l’impact du dispositif sur la qualité de vie des utilisateurs
Points clés du poste de référent·e scientifique :
- Statut : contractuel
- Spécialité/domaine : sciences humaines et sociales dont sociologie et psychologie
- Contrat : CDD
- Quotité souhaitée : temps plein
- Durée du contrat : 18 mois, prolongation possible en fonction des résultats obtenus
- Date de prise de poste souhaitée : premier trimestre 2026
- Lieu : Centre d’excellence iMIND (Campus hospitalier Le Vinatier, Bron, France), avec des déplacements dans la Métropole de Lyon à prévoir
- Télétravail : 1 jour de télétravail possible
- Salaire mensuel brut : selon grille salariale du Centre Hospitalier Le Vinatier
Sous la co-direction d’Amélie Soumier et de Marie Piéron et en lien avec l’équipe opérationnelle iMIND, le·la post-doctorant·e aura un rôle stratégique, en tant que référent·e scientifique des trois études. À ce titre, il·elle sera notamment chargé·e de :
- Concevoir et mettre en place les protocoles de recherche pour les trois volets d’étude :
- Définition des plans d’échantillonnage, méthodes de recueil de données, outils d’évaluation (questionnaires standardisés, mesures comportementales, enquêtes)
- Dépôt et suivi des démarches éthiques si nécessaire (CPP, RGPD)
- Coordonner la mise en œuvre des études en lien avec les partenaires scientifiques, hospitaliers et techniques du projet (Le Vinatier, iMIND, ISC Marc Jeannerod, Université Lyon 2, Mengrov)
- Assurer l’analyse des données, quantitatives et qualitatives, issues de l’application et des enquêtes (analyse statistique longitudinale, régressions, traitement de données complexes)
- Encadrer des étudiant·es en Master 2 ou en thèse de 3e cycle (1 par étude) tout au long du projet
- Produire les livrables scientifiques (rapports bimestriels, articles scientifiques, communications)
Profil recherché :
Compétences attendues :
- Expérience avérée avec publications dans la mise en place de protocoles de recherche, y compris en terrain écologique ou en milieu clinique
- Maîtrise des outils d’analyse statistique (R, Python, ou équivalents)
- La maîtrise des méthodes qualitatives serait un plus.
Connaissances :
- Familiarité avec les problématiques de neurodiversité, troubles du neurodéveloppement, ou accessibilité urbaine appréciée
- L’expertise d’usage est la bienvenue
Savoir être :
- Capacité de coordination
- Capacité d’adaptation
- Excellent relationnel
Le détail complet de l’offre se trouve sur la fiche de poste.
Pour postuler, envoyez votre CV, votre lettre de motivation et un ou deux exemples de publications ou rapports scientifiques à Amélie Soumier (amelie.soumier@isc.cnrs.fr) et Marie Piéron (marie.pieron@cnrs.fr) et Caroline Demily (caroline.demily@ch-le-vinatier.fr) avant le 20 février 2026.
Annonce iMIND

A lire également
Divercity
Avec le dispositif Divercity, l’objectif est de créer un écosystème adapté aux particularités des personnes avec des troubles du neurodéveloppement, avec l’appui et le concours d’un réseau de lieux publics et de commerçants sensibilisés et répertoriés sur une application mobile participative.
En savoir plus
Autisme : les différences entre filles et garçons sont-elles présentes dès la naissance ?
Les débats sont animés au sujet des manifestations genrées du trouble du spectre de l’autisme (TSA). De fait, beaucoup de filles et de femmes autistes passent inaperçues, malgré des difficultés dans la communication et les interactions sociales. Le DSM-5, l’un des principaux ouvrages de classification psychiatrique, estime d’ailleurs qu’il y aurait 1 femme autiste diagnostiquée pour 4 hommes autistes. Est-ce parce qu’il y a réellement moins de femmes que d’hommes autistes, ou est-ce dû à des manifestations différentes du trouble selon le genre et/ou le sexe ? Un précédent article d’iMIND avait déjà exploré la question du sous-diagnostic des femmes autistes en parlant de “signes” d’autisme moins reconnaissables et de la tendance des femmes autistes à mieux dissimuler leurs particularités.
Considérant l’hétérogénéité du TSA, des chercheur·euse·s du Centre d’excellence sur l’autisme de l’Université de Californie à San Diego ont décidé d’étudier les différences entre les sexes chez des jeunes enfants autistes de 12 à 48 mois. Étudier ces différences dès le plus jeune âge permettrait entre autres de limiter les biais induits par le camouflage social et d’observer les variations du trouble quand il est visible.

Comment l’équipe de recherche a-t-elle procédé ?
La population étudiée
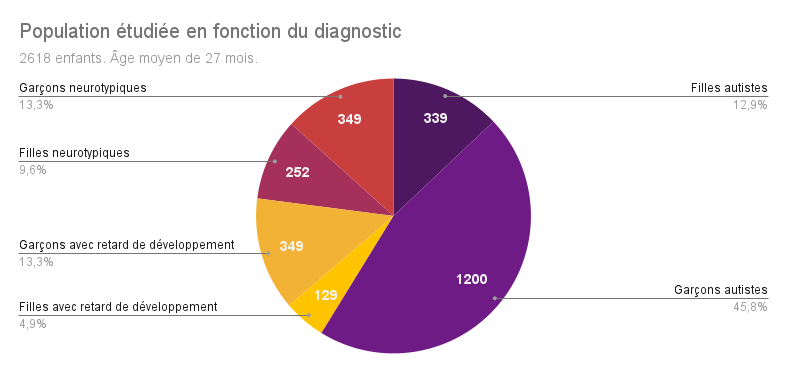
D’autres études sur le sujet ont déjà été effectuées, mais leurs résultats divergent grandement en raison de la taille de la population étudiée, de la durée de l’étude ou encore des méthodes employées. Ici, les chercheur·euse·s de San Diego ont pu suivre 2618 enfants de 12 à 48 mois entre 2002 et 2022. 75% d’entre eux avaient été repérés grâce au modèle Get SET Early®, un programme états-unien de dépistage de l’autisme dès 12 mois lors des visites de contrôle chez le ou la pédiatre. Les 25% d’enfants restants avaient été adressés au Centre pour une évaluation de leur développement. Dans chaque cas, les parents ont participé au dépistage en remplissant le questionnaire Communication and Symbolic Behavior Scales Developmental Profile™ Infant-Toddler Checklist.
Passé ce dépistage initial, des professionnel·le·s de santé ont effectué 18 tests chez chaque enfant afin notamment de diagnostiquer un potentiel autisme, mais aussi d’évaluer les compétences sociales, la compréhension et l’expression orale, la gestuelle, la motricité et de la perception visuelle.
Lors d’un dépistage, on utilise des échelles dont la sensibilité permet de repérer la plupart des personnes autistes. Elles permettent de ne pas passer à côté de cas, mais peuvent aussi identifier à tort certaines personnes non autistes : on parle alors de faux positifs. Le dépistage permet d’orienter les professionnel·le·s vers un diagnostic.
Lors d’un diagnostic, on utilise des échelles dont la spécificité permet de confirmer avec précision la présence de l’autisme. Cependant, elles peuvent parfois ne pas détecter certaines personnes avec une forme plus discrète : on parle alors de faux négatifs. Le diagnostic permet de confirmer la présence ou non d’un TSA.
⇒ Les échelles de dépistage et de diagnostic ont toutes deux leurs atouts et leurs faiblesses. Une évaluation clinique doit toujours être nuancée.
À l’issue des tests diagnostiques, les jeunes enfants ont été séparés en trois groupes : les enfants autistes, les enfants avec un retard de développement et les enfants neurotypiques (au fonctionnement neurologique considéré dans la norme).
Les analyses menées
Les chercheur·euse·s ont mené trois types d’analyse :
- une comparaison entre les filles et les garçons à un moment fixe,
- une comparaison classant tous les enfants par niveau de performance,
- une comparaison entre les filles et les garçons sur le temps long.
Comparaison entre les filles et les garçons de chaque groupe
En premier lieu, les chercheur·euse·s ont analysé les différences entre les sexes pour chaque groupe d’enfants. En effet, chercher les différences seulement entre les filles et les garçons autistes aurait été une démarche incomplète : il faut pouvoir comparer avec les enfants neurotypiques. Pour effectuer ces comparaisons, l’équipe de recherche a inclus des données relevées à différents moments, afin de limiter les effets liés aux âges différents des participant·e·s.
Chez les enfants autistes, les garçons avaient des scores inférieurs à ceux des filles dans le questionnaire de dépistage rempli par les parents. Cependant, dans 17 tests diagnostiques sur 18, les chercheur·euse·s ont noté qu’il n’y avait pas de différences significatives entre filles et garçons. La seule différence se trouvait au niveau des compétences dans la vie quotidienne, évaluées par les Vineland Adaptative Behavior Scales, où les filles avaient un meilleur score.
Chez les enfants ayant un retard de développement, il n’y avait pas non plus de différences significatives entre filles et garçons.
Chez les enfants neurotypiques en revanche, les garçons avaient des performances moindres que les filles à la fois dans le questionnaire de dépistage rempli par les parents et dans 10 des tests diagnostiques effectués par les professionnel·le·s de santé. Les filles neurotypiques avaient de meilleurs scores dans des domaines comme la motricité fine, le langage ou la perception visuelle.
Comparaison par niveau de performance des nourrissons
Plutôt que de simplement en rester à des comparaisons entre filles et garçons autistes, neurotypiques et avec un retard de développement, les chercheur·euse·s ont essayé de comparer tous les enfants, peu importe à quel groupe ils ou elles appartenaient. L’équipe de recherche a utilisé la Similarity Network Fusion (SNF), une méthode algorithmique permettant de regrouper les profils qui vont naturellement ensemble en combinant le plus de données possible. Ici, des mesures de signes de l’autisme (avec l’Autism Diagnostic Observation Schedule, ou ADOS), du comportement adaptatif – autonomie, communication – (avec les Échelles de comportement adaptatif Vineland) et du développement cognitif (avec les Mullen Scales of Early Learning, ou MSEL) ont été utilisées.
La Similarity Network Fusion (SNF) est une technique d’analyse par grappe : les profils des enfants ont été examinés dans le but de déterminer les regroupements naturels en fonction des performances sociales, motrices ou langagières.
Cette analyse par grappe a eu lieu en deux étapes :
- Tout d’abord, on a pris 80% des enfants (1337) et la SNF a permis de constater qu’il était possible de les classer en trois groupes selon leur niveau de performance (élevé, moyen ou faible). Ces enfants ont permis d’avoir des données d’entraînement pour le modèle pendant sa conception.
- Ensuite, ces trois groupes ont été étendus aux 20% d’enfants restants afin de valider la pertinence du modèle. Ces enfants ont permis de tester le modèle une fois qu’il a été créé (données de test).
Les groupes n’ont été formés qu’avec les données de trois tests différents (ADOS, Vineland et MSEL). Toutefois, les chercheur·euse·s ont aussi utilisé les mesures récoltées par d’autres tests (les variables externes) afin d’être plus exhaustif·ve·s.
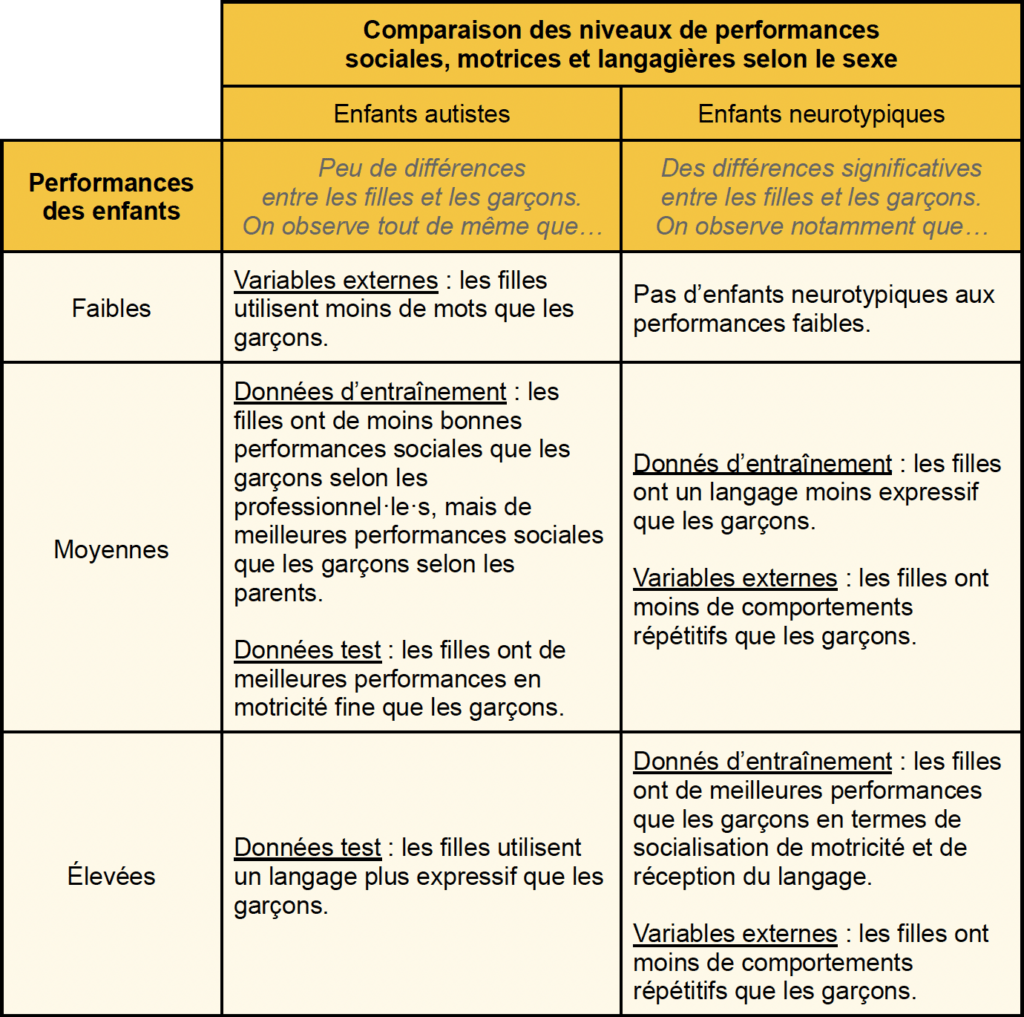
Il semblerait donc que les filles et les garçons autistes se ressemblent bien plus entre eux que les filles et les garçons neurotypiques, malgré quelques éléments allant globalement dans le sens de meilleures capacités pour les filles peu importe la catégorie.
Analyses sur le long terme
Enfin, les chercheur·euse·s ont effectué une analyse dans la durée, en observant la trajectoire des enfants autistes et des enfants neurotypiques à travers le temps (de 12 à 48 mois).
Chez les enfants autistes, il n’y avait pas de différence au début ; mais dans le temps, les résultats des garçons montraient une dégradation progressive des compétences sociales.
Chez les enfants neurotypiques, les filles avaient de bien meilleurs scores au début concernant la socialisation, la perception visuelle et le comportement. Elles présentaient aussi moins d’intérêts restreints. Sur le temps long, les filles s’amélioraient également plus que les garçons.
Quelles sont les conclusions de cette étude ?
De manière générale, chez les enfants de 12 à 48 mois, il semblerait que les filles et garçons autistes soient bien plus proches entre eux comparativement aux filles et aux garçons neurotypiques. Les quelques différences relevées selon le sexe parmi les jeunes enfants autistes ne sont en effet pas statistiquement significatives.
Ce résultat va à l’encontre d’autres études sur le sujet. Selon les auteur·ice·s de l’étude, cela peut s’expliquer de deux manières :
- une première hypothèse incrimine les études précédentes : il se peut qu’elles aient eu des problèmes de méthodologie (taille des échantillons, mesures choisies) ;
- une seconde hypothèse propose que les différences entre les sexes n’existent pas au moment où les signes de l’autisme apparaissent, mais qu’elles surviennent par la suite en raison de facteurs psychosociaux (comme l’engagement des parents) ou biologiques (comme les hormones) lors du développement.
Recontextualisation de l’étude
Pour approfondir la compréhension et confronter différentes perspectives, nous avons interrogé Adeline Lacroix, docteure en neurosciences, dont le travail sur l’autisme a toujours été parcouru par la question des différences liées au sexe et au genre. Cette rencontre nous a permis d’obtenir un regard critique sur cette récente étude et de la recontextualiser.
Adeline Lacroix est chercheuse en neurosciences. Suite à l’annonce de son diagnostic d’autisme, elle reprend des études en psychologie et soutient sa thèse à Grenoble en 2022, dans laquelle elle s’intéresse à la perception des visages dans l’autisme. Ses travaux se penchent sur les différences liées au sexe et au genre dans l’autisme, une thématique qu’elle poursuit actuellement dans le cadre d’un post-doctorat au Canada. |
Comment interpréter les résultats ?
Un raisonnement circulaire au niveau du recrutement des participants à l’étude
Selon Adeline Lacroix, les résultats sont potentiellement restreints à une certaine population autiste, et la population étudiée ne représente pas forcément tout le spectre. Les enfants ont été classés en deux groupes distincts : d’une part les neurotypiques, et d’autre part les enfants présentant un TSA. Or, ces enfants autistes ont toutes et tous été diagnostiqué·e·s, ce qui signifie qu’ils et elles atteignent déjà un score seuil à certaines échelles de dépistage et de diagnostic. Cette démarche ne permet donc pas de prendre en compte tout le spectre, puisqu’une partie des personnes autistes ne reçoivent un diagnostic que plus tardivement.
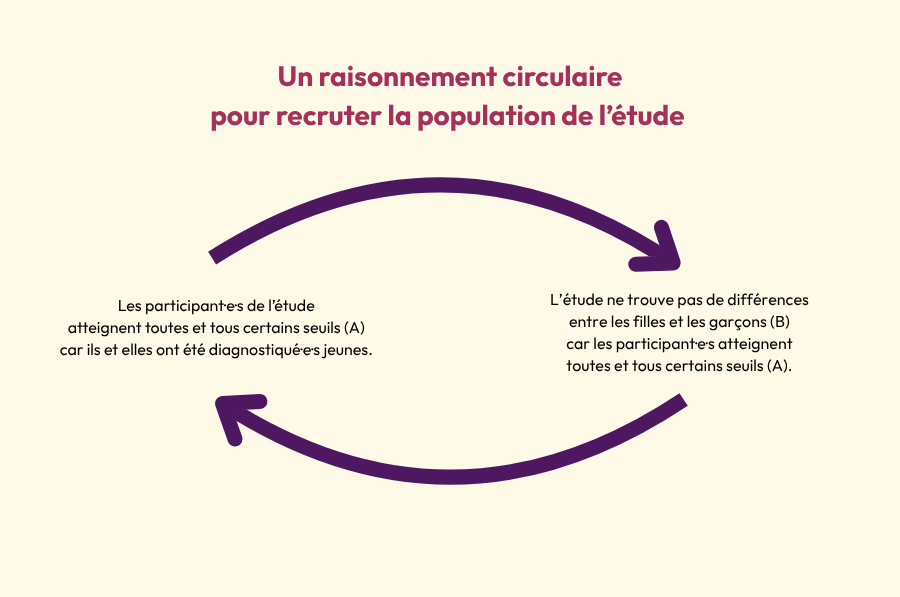
L’équipe de recherche elle-même indique que son étude ne prend pas en compte toutes les personnes autistes à haut niveau de fonctionnement : elles passeraient entre les mailles du programme Get SET Early®. De même, les outils diagnostiques utilisés pourraient ne pas repérer une partie des profils féminins.
Ainsi, il faut modérer l’interprétation de l’étude quant à la partie du spectre concernée. Le fait qu’il n’y ait pas de différences entre les sexes pour les jeunes enfants autistes est peut-être observable pour cette population, mais le résultat n’est pas forcément extrapolable à tout le spectre de l’autisme.
Adeline Lacroix mentionne une étude de Chawarska qui obtenait des résultats contradictoires. Dans celle-ci, on avait suivi des enfants à haute ou basse probabilité d’être autiste selon qu’ils ou elles aient un frère ou une sœur autiste. L’autisme ayant une forte composante génétique, il est plus fréquent pour une personne de présenter des traits autistiques ou d’être autiste si sa famille comporte des personnes autistes.
Dans cette étude, des différences précoces étaient déjà observées entre les filles et les garçons à forte probabilité d’être autiste – notamment par eye-tracking, où les filles avaient déjà une plus forte attention pour les visages que les garçons. Il est donc possible qu’il existe déjà des processus de compensation au plus jeune âge.
Cette étude a toutefois elle aussi des limites : elle se base sur le suivi de personnes à haute ou basse probabilité d’être autiste (et non pas sur le suivi de personnes autistes à proprement parler), et la population étudiée est bien plus restreinte. Cependant, il est intéressant de croiser les sources, puisque toutes les études ont leurs limites et qu’on ne peut pas tirer de raisonnement hâtif.
Des trajectoires développementales différentes chez toutes et tous
Revenons à l’étude de départ, qui suppose que les différences entre filles et garçons autistes apparaissent avec le temps, sous des effets biologiques et/ou sociaux. Adeline Lacroix appuie cette hypothèse, mais insiste sur le fait que les différences liées au sexe et au genre s’appliquent à toutes et tous, autistes comme non-autistes. Elles peuvent certes impacter les manifestations de l’autisme, mais elles ne sont pas propres à l’autisme.
D’où vient le biais genré dans l’autisme ?
Un biais de la part des clinicien·ne·s…
S’il y a des manifestations parfois différentes de l’autisme chez les hommes et les femmes, il faut noter qu’un biais de la part des clinicien·ne·s est possible. Adeline Lacroix pose l’hypothèse d’un mécanisme autoentretenu lié à un biais historique dans l’étude de l’autisme. Comme les premières descriptions de l’autisme ont été basées sur l’observation de jeunes garçons, les clinicien·ne·s n’ont pas toujours connaissance de l’existence de femmes autistes et pourraient avoir des difficultés à repérer ces dernières. On fait donc moins de recherche sur les femmes autistes de tout le spectre, et les femmes diagnostiquées sont celles qui correspondent aux seuils pensés pour les hommes. On pourrait donc passer à côté d’une partie du spectre de l’autisme. Dans son livre Autisme au féminin, Adeline Lacroix souligne que parmi les témoignages, une des caractéristiques communes à de nombreuses femmes autistes est d’avoir reçu des diagnostics psychiatriques erronés avant d’arriver sur la piste de l’autisme.
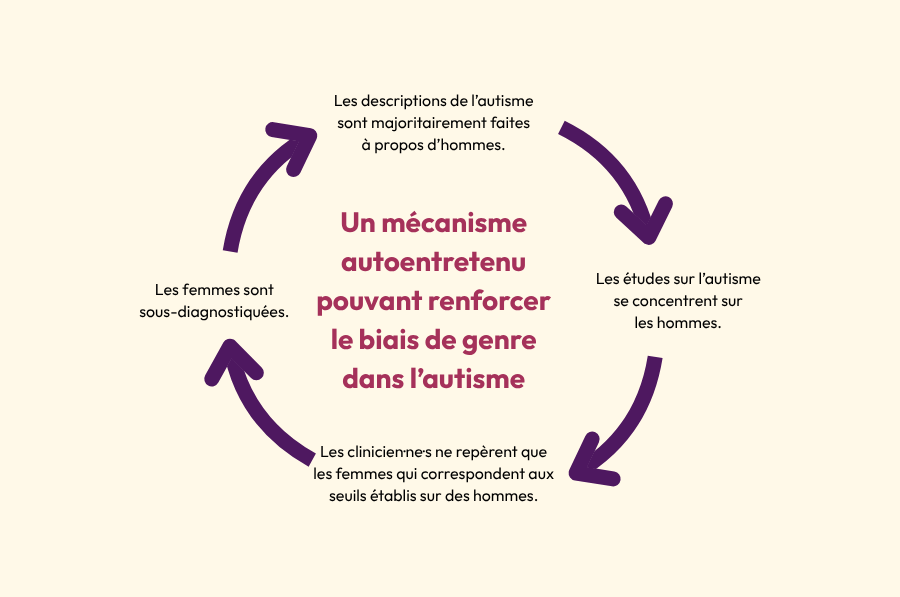
…mais aussi du reste de la société
Ce biais genré pourrait ne pas se limiter aux clinicien·ne·s. Adeline Lacroix nous fait part d’une étude de Whitlock au cours de laquelle des chercheur·euse·s ont présenté des vignettes cliniques à du personnel éducatif d’école primaire. Chaque vignette comprenait un prénom masculin ou féminin, ainsi que la description d’un profil qui pouvait rappeler l’autisme, le TDAH ou l’anxiété de séparation. Certains profils correspondaient à un autisme plus “féminin” et d’autres à un autisme plus “masculin”. Si le profil autistique était plus “masculin” le personnel éducatif pensait plus vite à proposer un suivi par un·e professionnel·le, quel que soit le genre du prénom sur la vignette. En revanche, si le profil autistique était plus “féminin”, le personnel éducatif avait plus de mal à identifier que l’enfant pouvait être autiste. Avec un prénom masculin et un “profil féminin”, le personnel éducatif supposait que l’enfant était peut-être autiste ; mais avec un prénom féminin et la même description, le personnel éducatif se posait significativement moins la question de l’autisme. Ainsi, à manifestation identique, si le profil est plus discret, les filles autistes sont beaucoup moins repérées par l’entourage que les garçons.
Quelles précautions prendre pour parler de cette étude ?
Les chercheurs de San Diego ont choisi d’étudier des jeunes enfants, ce qui apporte un réel intérêt quant aux travaux sur l’autisme au féminin car il s’agit d’un âge où les stratégies de camouflage social existent peu ou pas. Toutefois, conclure qu’il n’y a pas de différences entre les filles et les garçons autistes chez les jeunes enfants de tout le spectre pourrait être précipité. Il serait plus juste de retenir de cette étude qu’à un âge précoce, pour les enfants qui ont un diagnostic précoce, les différences existent peu.
⇒ Un profil plus discret ou moins remarquable à cet âge peut tout à fait relever du TSA.
Ressources
- Étude des chercheur·euse·s de San Diego
- Article d’iMIND : TSA et genre : pourquoi les femmes autistes sont-elles sous-diagnostiquées ?
- Article sur l’outil de dépistage de l’autisme Get SET Early®
- Définition de l’analyse par grappes
- Étude sur les différences entre les sexes chez des enfants à haute ou basse probabilité d’être autiste
- Étude sur la reconnaissance des signes de l’autisme par du personnel éducatif
- Article d’iMIND : Autisme et diversité de genre
- Journée iMIND #3 – Explorer les diversités : à l’intersection des identités trans et de l’autisme

Autisme et diversité de genre
Contexte de l’étude
Une corrélation possible entre trouble du spectre de l’autisme et identité de genre ?
Le trouble du spectre de l’autisme (TSA) est un trouble du neurodéveloppement (TND) qui impacte notamment la communication et les interactions sociales. Il peut influencer la manière dont une personne perçoit et exprime son identité, y compris son identité de genre. Le genre est une construction sociale : il correspond aux rôles, comportements et attentes qu’une société attribue aux personnes en fonction de leur apparence ou de leur sexe assigné à la naissance, et il peut varier selon les cultures et les époques.
Dans ce contexte, il semble pertinent d’examiner les liens entre autisme et genre. Des clinicien·ne·s-chercheur·euse·s comme Élodie Peyroux, PhD, et le Dr Guilhem Bonazzi, du pôle Hospitalo-Universitaire Autisme, neuroDéveloppement et Inclusion Sociale (HU-ADIS) du Vinatier, ont observé dans leur pratique que de nombreuses personnes autistes s’identifient en dehors des normes de genre traditionnelles. Cela signifie que leur genre ressenti ne correspond pas toujours à celui qui leur a été assigné à la naissance, ce qui les place au sein de la diversité de genre. Cette observation invite à mieux comprendre comment se construit l’identité de genre pour les personnes autistes.

L’accompagnement en affirmation de genre au pôle HU-ADIS
Les professionnel·le·s du pôle HU-ADIS ont décidé de systématiser leur approche en créant l’unité CASCADE (consultations d’accompagnement en santé psychique pour les adultes divers de genres). Cette unité reçoit des personnes diverses de genre de 16 ans et plus, que ce soit pour un avis global en santé mentale, un accompagnement en affirmation de genre ou des consultations à visée diagnostique si nécessaire.
L’accompagnement en affirmation de genre contribue à la reconnaissance des personnes trans, à leur bien être et à leurs droits. L’affirmation de genre peut notamment revêtir des aspects sociaux (par ex. avec un changement de prénom), médicaux (par ex. avec une hormonothérapie) ou encore légaux (par ex. avec un changement sur l’état civil).


Lorsqu’une personne majeure entre dans un parcours d’affirmation de genre médical, elle peut consulter sur demande. Pour les mineur·e·s, en revanche, un avis médical en santé mentale reste la règle. Dans la région lyonnaise, les mineur·e·s de moins de 16 ans peuvent s’adresser à l’unité VAGUE (variance de genre, unité enfants).
Le début d’un projet de recherche
En se penchant sur l’intersection entre TSA et diversité de genre, les chercheur·euse·s ont constaté que beaucoup d’études scientifiques étaient davantage orientées sur les traits autistiques des personnes diverses de genre, et non sur la diversité de genre chez les personnes autistes.
Par exemple, une étude (Mazzoli et al., 2022) a mis en évidence la présence de traits autistiques chez certaines personnes diverses de genre. Toutefois, ces traits semblaient diminuer après le début d’une hormonothérapie. Si cette hypothèse se confirmait, cela suggérerait que les traits autistiques pourraient, dans certains cas, être un épiphénomène – c’est-à-dire une conséquence ou une expression secondaire liée à la situation de diversité de genre.
De plus, dans les études précédentes, le genre était étudié sous le prisme d’une classification médicale, sous les appellations de « troubles de l’identité sexuelle » et de « dysphorie de genre ».
Explorer l’articulation entre les identités de genre et le TSA pourrait permettre de mieux accompagner les personnes autistes. Les chercheur·euse·s du pôle HU-ADIS se sont interrogé·e·s sur la proportion de personnes autistes concernées par la diversité de genre et se sont fixé trois objectifs :

Quelle a été la démarche suivie par les chercheur·euse·s ?
L’équipe de recherche a compilé de nombreuses études, pour réaliser ce que l’on appelle une revue systématique. Le but d’un tel travail est de synthétiser les connaissances sur un sujet. Par la suite, les chercheur·euse·s ont effectué une méta-analyse, c’est-à-dire qu’ils et elles ont pris les données chiffrées des études pour opérer des analyses statistiques.
Il s’agit d’une méthodologie similaire à celle que d’autres chercheur·euse·s du pôle HU-ADIS avaient employée pour étudier la corrélation entre le TDAH et le sans-abrisme.
Les méta-analyses et les revues systématiques sont généralement considérées comme fournissant un niveau élevé de preuve scientifique.
En s’appuyant sur l’analyse rigoureuse d’un grand nombre d’études, soigneusement sélectionnées, elles offrent une fiabilité accrue des résultats et des conclusions
Différents critères ont été définis afin d’identifier les études à retenir :
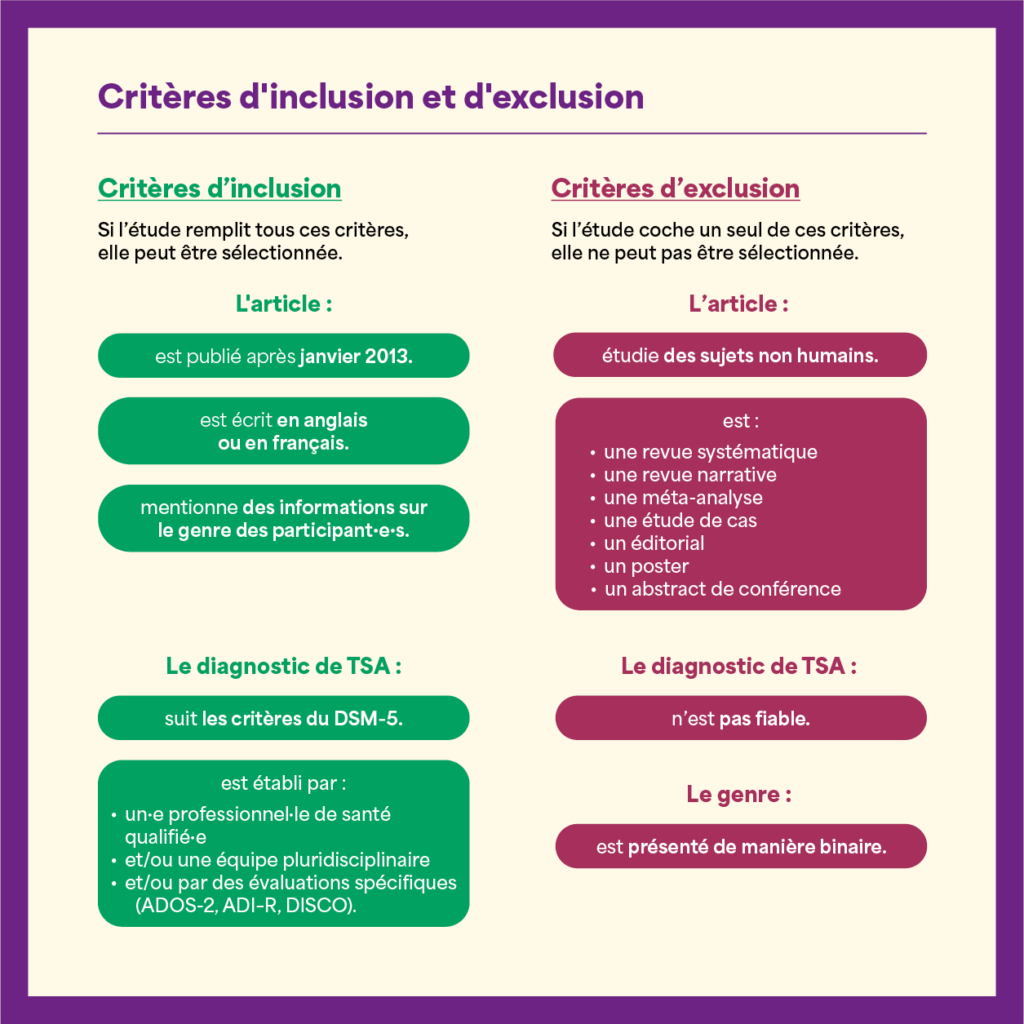
Sur plus de 7 000 études identifiées, seule une vingtaine ont été conservées après application des critères de sélection.
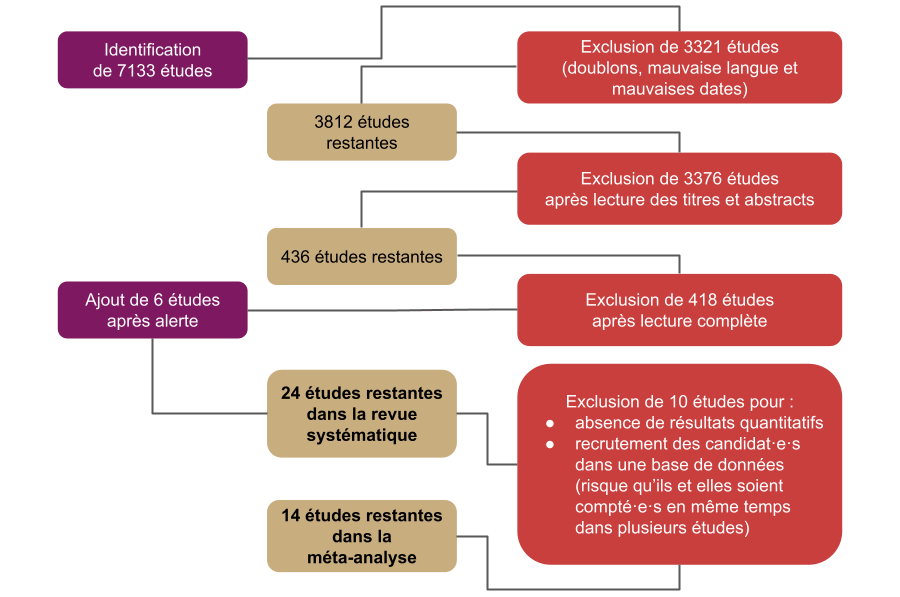
Quels ont été les résultats ?
Les résultats de la méta-analyse permettent d’estimer que 7,37 % des personnes autistes présenterait une diversité de genre. Toutefois, cette moyenne résulte de données très hétérogènes selon les études, avec des proportions variant de 0,85 % (Graham Holmes et al., 2020) à 27,27 % (Chang et al., 2022).
Cette différence pourrait s’expliquer par la manière dont la diversité de genre a été envisagée, mais aussi par les définitions du genre utilisées. En effet, certaines études avaient une définition binaire du genre : elles envisageaient uniquement que les participant·e·s se sentent appartenir à leur genre assigné ou au genre « opposé » à celui qu’on leur avait assigné à la naissance. À l’inverse, les études qui avaient une définition moins binaire du genre permettaient plus de fluidité dans les réponses.
Que faire face à de tels écarts ?
Face aux fortes variations des résultats d’une étude à l’autre, l’équipe a décidé de poursuivre ses investigations pour tenter de comprendre les raisons de telles disparités. Lors de ces analyses complémentaires, l’équipe s’est notamment interrogée sur la manière dont le diagnostic de TSA avait été posé. Cet élément ne semblait toutefois pas influencer le pourcentage de personnes autistes diverses de genre.
En revanche, deux critères sont ressortis. D’une part, du côté des études, l’objectif de recherche influence significativement les résultats trouvés. Quand une étude a pour objet le genre, le pourcentage de personnes autistes diverses de genre est bien plus élevé. L’équipe de recherche suppose que ces différences viennent de critères mieux établis pour caractériser la diversité de genre. D’autre part, du côté des personnes, le genre assigné à la naissance influence aussi les résultats trouvés, mais cette influence n’est pas significative. Les personnes autistes assignées filles à la naissance feraient plus souvent partie de la diversité de genre que les personnes autistes assignées garçon à la naissance, mais la puissance statistique de l’étude ne permet pas d’affirmer ce résultat.
Le « genre assigné à la naissance » est le genre enregistré de quelqu’un à la naissance. Il est le plus souvent établi en fonction des organes génitaux externes d’une personne : pénis pour l’homme, vulve pour la femme.
On emploie souvent les termes AFAB, pour assigned female at birth (assigné·e fille à la naissance) ; et AMAB, pour assigned male at birth (assigné·e garçon à la naissance).
Le genre assigné à la naissance ne correspond pas forcément à l’identité de genre d’une personne.
La corrélation entre TSA et diversité de genre est-elle une simple coïncidence ?
L’équipe du pôle HU-ADIS a relevé différentes hypothèses expliquant le potentiel lien entre TSA et diversité de genre. Elles se déclinent en trois catégories (Van Der Miesen et al., 2016) : les théories biologiques, psychologiques et sociales.
Selon certaines théories biologiques, les personnes autistes auraient un niveau de testostérone très élevé avant la naissance. Ce haut niveau influencerait le développement de leur cerveau : on parle d’ailleurs d’« extreme male brain », soit une forme extrême du cerveau masculin. Ainsi, les personnes autistes auraient du mal dans les activités perçues comme « plus féminines » (ce qui comprend les interactions sociales). Il y aurait moins de différences entre les hommes et les femmes autistes qu’entre les hommes et les femmes neurotypiques. Ces théories, n’ont cependant a l’heure actuelle jamais été validées par des données scientifiques.
Pour les théories psychologiques, ce seraient certaines particularités liées à l’autisme (comme les déficits en théorie de l’esprit, la rigidité ou les comportements obsessionnels) qui pourraient être à l’origine de la diversité de genre observée dans cette population. Par exemple, certain·e·s auteur·rice·s mentionnent que les difficultés à se percevoir soi-même et à se représenter les états mentaux de soi et d’autrui, en lien avec les difficultés de théorie de l’esprit, pourraient impacter la représentation de l’identité de genre, chez les personnes avec autisme. D’autres hypothèses s’intéressant à l’impact de la rigidité cognitive proposent que les enfants avec autisme conserveraient une croyance de genre très stéréotypée, même en grandissant, ce qui pourrait constituer la base de la diversité de genre dans cette population.
Enfin, les théories sociales insistent sur le caractère socialement construit du genre et expliquent la diversité de genre des personnes autistes par leur fonctionnement social non normatif. Il se pourrait, par exemple, que les personnes ayant un TSA résistent davantage au conditionnement social genré.
La revue ne cherche toutefois pas à établir la véracité de ces théories. Les chercheur·euse·s insistent d’ailleurs sur le besoin de conduire un plus grand nombre d’études, afin de mieux comprendre ces interactions.
Quelles ont été les difficultés rencontrées ?
L’équipe du pôle HU-ADIS a fait face à plusieurs obstacles pour réaliser sa revue, notamment le manque d’études sur le long terme et le manque de comparaisons entre personnes autistes et personnes neurotypiques.
De plus, l’identité de genre est un angle de recherche relativement nouveau dans le domaine. Certaines études étaient plus binaires que d’autres : elles manquaient donc de choix possibles dans les réponses proposées aux participant·e·s pour qualifier leur identité de genre. D’autres études excluaient de facto les personnes diverses de genre de leur protocoles. Enfin, il est aussi possible que des personnes diverses de genre se soient autocensurées ou n’aient pas participé à des études.
Un biais de publication a donc été mis en évidence. Il est plus que probable que l’on sous-estime la prévalence de la diversité de genre dans l’autisme pour ces différentes raisons. D’ailleurs, en appliquant des méthodes de correction des biais de publication, la prévalence de la diversité de genre augmente, ce qui montre que le chiffre annoncé plus haut (7,3 % des personnes autistes seraient diverses de genre) n’est pas surestimé.
Quelles suites pour l’étude ?
D’une part, Clara Gloanec, une interne du pôle, s’est intéressée à la manière de poser les diagnostic d’autisme chez les personnes diverse de genre. Pour sa thèse de médecine, elle a réalisé une méta-analyse et une revue systématique mettant en évidence que les outils utilisés sont le plus souvent des questionnaires de dépistage ou des autodiagnostics, permettant assez mal de définir les populations.
D’autre part, Élodie Peyroux, PhD, et le Dr Guilhem Bonazzi poursuivent leurs travaux afin de mieux appréhender la manière dont l’identité de genre se construit chez les personnes autistes appartenant à la diversité de genre. Pour explorer cette question, il et elle réalisent des entretiens qualitatifs avec des personnes autistes de tous âges, sexes et genres, afin d’identifier leurs points communs, leurs différences, ainsi que la façon dont chacun·e perçoit et vit son identité de genre.
Ressources
- Journée iMIND #3 – Explorer les diversités : à l’intersection des identités trans et de l’autisme
- Étude du Dr Guilhem Bonazzi et d’Élodie Peyroux, PhD
- Études citées dans l’article :
- Chang et al., 2022 – Étude retenue dans la revue systématique/méta-analyse et trouvant la plus grande proportion de personnes diverses de genre dans l’autisme (27,27 %)
- Graham Holms et all, 2020 – Étude retenue dans la revue systématique/méta-analyse et trouvant la plus petite proportion de personnes diverses de genre dans l’autisme (0,85 %)
- Mazzoli et al., 2022 – Étude montrant que l’hormonothérapie peut parfois diminuer les traits autistiques chez des personnes diverses de genre
- Van Der Miesen et al., 2016 – Étude reprenant les différentes théories expliquant le lien entre TSA et diversité de genre.

Les personnes sans domicile sont-elles plus concernées par le TDAH ?
TDAH et sans-abrisme : une corrélation peu étudiée
Ne pas avoir de domicile fixe peut engendrer ou renforcer de multiples problèmes de santé. Curieusement, malgré le fait que l’on dénombre environ 150 millions d’enfants vivant à la rue dans le monde, les enfants et les adolescent·e·s sans domicile font l’objet de peu d’études sur leur santé et leur bien-être.
Nous avons interrogé la professeure Caroline Demily et le docteur Charles Denis, du pôle hospitalo-universitaire Autisme, neuroDéveloppement et Inclusion Sociale (HU-ADIS) du Vinatier, qui se sont intéressé·e·s à cette question.

Tout a commencé par une observation de la Professeure Demily qui a été frappée par la présence importante de personnes sans domicile fixe (SDF) présentant des comportements évocateurs de troubles du neurodéveloppement (TND), tels que le trouble du déficit de l’attention avec ou sans hyperactivité (TDAH) ou l’autisme. Elle évoque notamment une personne qui passait ses journées à écrire au sujet d’une planète. Cela a fait germer l’idée d’un projet de recherche. En effet, on sait que d’une part, les personnes SDF sont une population relativement peu étudiée et chez qui les troubles psychiques sont surreprésentés ; d’autre part, beaucoup de TND sont diagnostiqués de manière erronée et vus comme des troubles psychiques.
Partant de ce paradoxe, le pôle HU-ADIS du Vinatier a décidé d’étudier le lien entre absence de domicile fixe et TDAH chez les enfants et adolescent·e·s (Denis et al., 2025).
Le TDAH fait partie des TND. Il comporte des symptômes d’inattention et d’hyperactivité ou d’impulsivité. Il concerne environ 5,9 % des enfants et adolescent·e·s. Avoir un TDAH augmente d’ailleurs le risque d’être SDF un jour dans sa vie. Une étude s’étalant sur 33 ans a observé que les hommes ayant un TDAH ont entre 3 et 4 fois plus de chance d’être confrontés à la perte de logement que les autres hommes (Murillo et al., 2016).
Établir un lien entre avoir un TDAH et être SDF permettrait d’informer les clinicien·ne·s et les autorités afin de mieux accompagner les populations concernées. La prise en charge du TDAH nécessite un suivi régulier, ce qui est difficile d’accès pour les personnes SDF.
Comment les chercheur·euse·s ont-ils procédé ?
Les chercheur·euse·s ont réalisé une revue systématique et une méta-analyse.
- Une revue systématique consiste à réunir le plus d’études scientifiques possible sur un sujet.
- Une méta-analyse consiste à prendre tous les résultats chiffrés de ces études afin de les mettre en commun.
Par ces deux procédés, les chercheur·euse·s limitent les biais car ils tirent leurs conclusions sur un large ensemble de cas. Mais pour cela, il a fallu établir certains critères de collecte afin de ne garder que les études pertinentes au regard du sujet.

Il a donc fallu passer au crible de nombreuses études pour vérifier si elles répondaient à ces critères. Sur 391 études recensées, seules 13 ont été retenues. Les données ont ensuite été compilées.
La qualité des études a été examinée grâce à des grilles d’évaluation.
Une batterie de tests statistiques a permis de conclure ou d’attester que les différences entre les études n’étaient pas dues au hasard ni à des biais de publication ou de taille d’échantillon. En effet, les études sur une petite population ont parfois des résultats drastiquement différents par rapport à celles effectuées sur des échantillons plus larges, ce qui peut biaiser la fiabilité en donnant l’impression qu’un phénomène est bien plus fort qu’il ne l’est en réalité.
Quelles ont été les difficultés rencontrées ?
La définition choisie pour le terme homeless n’était pas toujours indiquée dans les études. Or, en anglais, homeless peut faire référence à une grande variété de situations, allant de la plus extrême (le sans-abrisme, où l’on n’est pas hébergé du tout) au fait de ne pas avoir de domicile fixe (où l’on reçoit parfois de l’aide médico-sociale). Ces situations peuvent aussi évoluer dans le temps et être impactées par les différents dispositifs mis en place dans les pays. Les chercheur·euse·s ont donc fait le choix d’une définition la plus englobante possible, notamment du fait du petit nombre d’études.
De plus, la méthodologie utilisée pour recenser les cas de TDAH n’a pas été la même dans chaque étude. Souvent, des échelles de dépistage (moins fiables) ont été favorisées par rapport à des échelles diagnostiques (plus fiables), ce qui complique l’interprétation des données.
Qu’a-t-on observé ?
La méta-analyse a mis en lumière une grande diversité des résultats. Le pourcentage des enfants et adolescent·e·s SDF ayant un TDAH oscillait entre 1,6 % dans une étude népalaise (Ojha et al., 2013) et 64,5 % dans une étude canadienne (Labelle et al., 2020). En France, il était estimé à 2,4 % (Roze et al., 2016). Afin de concilier ces résultats, une moyenne pondérée a été effectuée, c’est-à-dire que l’on a pris en compte la taille des populations de chaque étude lors du calcul. Selon cette méta-analyse, la prévalence du TDAH atteindrait 22,8 % chez les enfants et adolescent·e·s SDF. Mais quel que soit le chiffre exact, il est bien supérieur à celui observé dans la population générale (5,9 % des enfants et adolescent·e·s).
Les chercheur·euse·s nous rappellent d’ailleurs que ces chiffres sont à prendre avec précaution. Ils indiquent plutôt une tendance qu’un résultat net en raison des différentes méthodologies employées.
Par ailleurs, on a observé que le paramètre ayant le plus d’impact sur la prévalence du TDAH chez les enfants et adolescent·e·s SDF était l’âge : on passe de 13,1 % d’enfants (moins de 12 ans) ayant un TDAH à 43,1 % d’adolescent·e·s (plus de 12 ans) ayant un TDAH. Les chercheur·euse·s pensent qu’un tel bond s’explique par l’environnement familial. En effet, dans toutes les études sauf une (Ojha et al., 2013), les enfants étaient à la rue avec leur famille tandis que les adolescent·e·s étaient seul·e·s.

Certaines de ces raisons poussant les adolescent·e·s à la rue peuvent être liées aux conséquences d’un TDAH, ou bien participer au développement ou à l’exacerbation des symptômes d’un TDAH.
Y a-t-il des choses à mettre en place pour contrer le phénomène ?
Cette méta-analyse invite à prendre en compte l’absence de domicile et le TDAH de manière plus globale. En effet, d’un côté, le TDAH et ses comorbidités peuvent renforcer la probabilité de devenir une personne SDF ; de l’autre, l’absence de domicile fixe peut exacerber les symptômes du TDAH. Il semble primordial de chercher à diagnostiquer au plus tôt, d’autant plus quand on sait qu’un retard de prise en charge peut augmenter le taux de mortalité. Les personnes SDF accèdent difficilement à des soins de santé : les réintégrer dans le système de soin est impératif.
En France, il existe des équipes mobiles psychiatrie-précarité (EMPP). Or, selon la professeure Demily, elles ne sont pas assez formées aux TND. La lecture très « psychiatrisante » peut donner lieu à des erreurs de diagnostic : un TDAH pourra être pris pour un trouble de la personnalité, ou un trouble du spectre de l’autisme (TSA) pourra être pris pour une schizophrénie. Selon elle, si l’on observe des problèmes d’addiction chez un jeune, la question du TDAH devrait systématiquement être posée (et il en va de même pour les difficultés d’insertion sociale, qui devraient au moins faire évoquer un TSA).
Le docteur Denis ajoute que ce manque de considération des TND est observé dans toute la psychiatrie adulte. Pour en arriver à la rue, « il y a souvent eu des ratés en amont ». Le passage à l’âge adulte est une période charnière pour les personnes ayant un TND, et on peut déplorer le manque d’accompagnements et d’aménagements.
Il faudrait donc développer les études de ce type, mais aussi s’intéresser aux trajectoires de vie pour identifier les ruptures de parcours.
Quelles suites pour l’étude ?
Le pôle HU-ADIS souhaite poursuivre ses recherches, cette fois-ci sur le terrain ! L’objectif sera de faire des évaluations diagnostiques chez des adultes SDF en Centre d’hébergement et de réinsertion sociale (CHRS). Comme ces personnes seront en CHRS, il sera plus facile d’effectuer un suivi et d’obtenir des résultats sur le temps long qu’avec des personnes sans-abris.
Trois TND seront recherchés : le TDAH, le TSA et le TDI (trouble du développement intellectuel). C’est donc une étude très ambitieuse qui se profile, mais qui permettra de poser un cadre théorique important. Il s’agira d’une première en France.
Ressources
- (Denis et al., 2025) Revue systématique et méta-analyse du pôle HU-ADIS au sujet de la prévalence du TDAH chez les personnes SDF
- (Labelle et al., 2020) Étude canadienne (prévalence de 64,5 %)
- (Murillo et al., 2016) Étude de 33 ans
- (Ojha et al., 2013) Étude népalaise (prévalence de 1,6 %)
- (Roze et al., 2016) Étude française (prévalence de 2,4 %)
La Coordination nationale TDAH Adultes vous convie au webinaire « TDAH et burn out, comprendre, diagnostiquer et prévenir », animé par le Dr Fulya Ozgun et son équipe. (Inscription en ligne avant le 9 mai)
Cette année, le GIS vous invite à vous former autour des TND en explorant la question des modélisations et méthodes expérimentales. Ces dernières peuvent-elles répondre aux enjeux des TND ?
L’Association pour la Recherche sur l’Autisme et la Prévention des Inadaptations vous invite pour une journée sur le thème « Vivre avec un TDAH, parcours de vie et complexités ».
La médiathèque du Bachut vous convie à une projection de Cassée Debout, avec la présence de Marie Rabatelle, dont la vie fait l’objet du film, et du SESSAD EVAI. (Inscription en ligne)
Des conférences, ateliers et tables rondes réuniront des spécialistes de tous horizons afin d’échanger au sujet des neurosciences. Un congrès à ne pas manquer pour découvrir les innovations d’un domaine d’avenir. (Inscription en ligne)
Pour financer ses projets, l’organisation Special Olympics France programme des courses solidaires dans tout le pays. C’est une occasion de célébrer la diversité en partageant les valeurs du sport.
Pour cette journée annuelle, la Société Française du TDAH a opté pour un programme axé sur les bonnes pratiques en termes de pharmacologie, de psychothérapie ou encore d’inclusion scolaire. (Inscription en ligne, distanciel possible)
À l’occasion de ce Congrès, les conférences et ateliers exploreront les TND et leur lien avec la scolarité. Les intervenants partageront leurs connaissances pour aider à bâtir l’école de demain ! (Inscription en ligne)
L’association Neuro’AtypiK vous invite à assister à une pièce de théâtre (Itinéraire d’un enfant coincé – sur inscription) puis à un salon rassemblant de nombreux acteurs en lien avec la thématique des TND.
La 20e édition du GREPACO, co-organisée par le Vinatier, le Centre iMIND et l’Université Lyon 2, portera sur les « interactions sociales à l’épreuve de la cognition ». Des conférences et ateliers pratiques seront organisés. (Inscription en ligne)
Pendant 3 jours, des conférences et ateliers aborderont le thème de la citoyenneté au quotidien. (Inscription en ligne, distanciel possible)

Identification d’un nouveau gène impliqué dans les troubles du neurodéveloppement : le gène DDX17
La recherche sur les troubles du neurodéveloppement (TND) vient de franchir un nouveau cap grâce à une collaboration internationale regroupant des équipes de recherche en France, au Royaume-Uni, en Allemagne, en Italie, en Islande et aux États-Unis. Publiés dans la prestigieuse revue Brain, ces travaux mettent en lumière le rôle du gène DDX17 dans le développement neuronal.
Retour sur cette découverte à la frontière entre génétique médicale et recherche fondamentale.

DDX17 : un gène au cœur de la régulation génique
Le gène DDX17 code pour une protéine appartenant à la famille des hélicases, qui sont impliquées dans la régulation de l’expression des gènes. Ces protéines jouent donc un rôle clé dans le contrôle des étapes menant à la synthèse des protéines, éléments constitutifs de la plupart de nos cellules humaines.
« Jusqu’à présent, nous étions surtout centrés sur de la recherche fondamentale autour des rôles de DDX17 dans la régulation des gènes », explique Cyril Bourgeois, qui a co-dirigé cette étude. « L’opportunité de collaborer avec des généticiens cliniques nous a permis d’explorer des applications directes de nos travaux. »
Les troubles du neurodéveloppement résultent d’une interaction complexe entre facteurs génétiques et environnementaux, dont les mécanismes précis restent encore largement méconnus. On estime aujourd’hui qu’environ 1 000 gènes sont impliqués dans ces troubles. Par ailleurs, l’influence de facteurs environnementaux est également étudiée pour mieux comprendre leur impact sur le développement cérébral. Grâce aux avancées en génomique, les chercheurs continuent d’affiner la liste des gènes impliqués et d’explorer les mécanismes biologiques sous-jacents, ouvrant ainsi la voie à de nouvelles approches diagnostiques et thérapeutiques. Cette étude sur le gène DDX17 permet de mettre en lumière un nouveau gène dont la mutation entraîne des conséquences neurodéveloppementales.
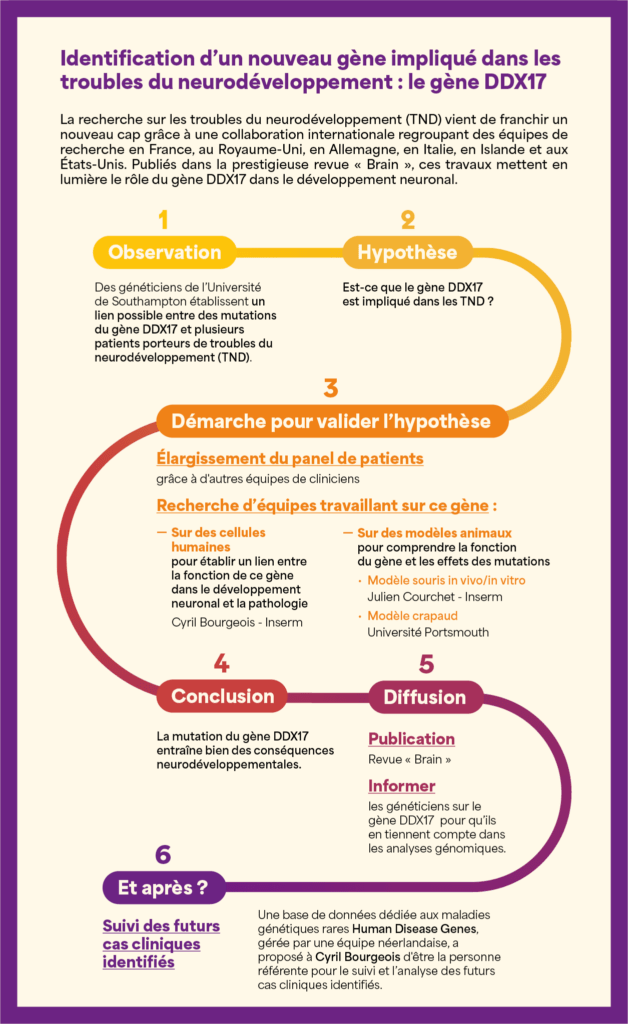
Une approche multidisciplinaire pour une découverte d’envergure
Tout a commencé quand une équipe de généticiens britanniques de l’Université de Southampton, dirigée par Sarah Ennis, a identifié le gène DDX17 comme un candidat d’intérêt dans les troubles du neurodéveloppement (TND). Grâce aux données issues du projet « 10 000 Genomes », ils ont établi un lien possible entre des mutations du gène DDX17 et plusieurs patients porteurs de TND, présentant un tableau clinique caractérisé notamment par une déficience intellectuelle, un retard de la parole et du langage, et un retard moteur, associé parfois à un syndrome autistique. Cependant, cette hypothèse nécessite une validation scientifique rigoureuse.
Ainsi, l’équipe britannique a entrepris d’élargir leur panel de patients présentant des mutations sur ce gène, et a par ailleurs sollicité une collaboration avec l’équipe de Cyril Bourgeois du Laboratoire de Biologie et Modélisation de la Cellule de l’ENS, qui travaillait déjà sur le gène DDX17. L’objectif de cette collaboration était d’établir un lien entre la fonction de ce gène dans le développement neuronal et cette nouvelle pathologie, afin de mieux en comprendre les causes au niveau cellulaire et moléculaire.
Une signature transcriptomique associée au neurodéveloppement
L’équipe de Cyril Bourgeois a tout d’abord mené une analyse transcriptomique sur des cellules humaines. Cette approche consiste à séquencer de manière exhaustive tous les ARN messagers de ces cellules, en comparant celles où le gène DDX17 est inactivé à celles où il ne l’est pas. Cette analyse, réalisée par une doctorante de l’équipe, Valentine Clerc, et par un ingénieur bio-informaticien, Xavier Grand, a permis d’identifier 350 gènes dont l’expression est dérégulée en l’absence du gène DDX17.
Une grande majorité de ces gènes est associée au développement morphogénique, et plus spécifiquement au développement neuronal, fournissant une piste sur le mécanisme pathologique sous-jacent chez les patients.

Des modèles animaux pour comprendre la fonction du gène et les effets des mutations
Fort de ces premières constatations, des recherches expérimentales sur des modèles animaux ont été réalisées afin de mieux comprendre les fonctions de DDX17 dans le développement cérébral.
Tout d’abord, Julien Courchet et son équipe ont utilisé une technique de micro-injection pour introduire, dans le cerveau d’embryons de souris en gestation, des molécules visant à inactiver ponctuellement le gène DDX17, sans le supprimer entièrement du génome, contrairement à un knock-out. Cette approche, plus rapide, permet d’obtenir des résultats en quelques semaines, contre plusieurs mois pour un knock-out. En suivant l’évolution du cerveau des souris de la période prénatale à la phase postnatale, Géraldine Meyer-Dilhet, ingénieure d’étude au sein de l’équipe, a observé des anomalies dans la croissance et la ramification des axones, signes d’un développement neuronal altéré.
Ces observations ont été confirmées par des expériences in vitro : Géraldine Meyer-Dilhet et Laloe Monteiro, deux ingénieures de l’équipe, et Martijn Kerkhofs, chercheur post-doctorant, ont mis en place des cultures neuronales issues de souris, dans lesquelles ils ont reproduit l’inhibition du gène en question. Les mêmes anomalies de croissance et de ramification ont été constatées, confirmant que l’altération se manifeste à la fois in vivo et in vitro.
Pour approfondir cette étude, des expériences de « rescue » (ou de sauvetage) ont aussi été réalisées: une copie fonctionnelle du gène DDX17 a été ré-introduite dans les cellules après son inactivation, ce qui a restauré le développement neuronal typique. Ces résultats renforcent l’idée que les altérations observées sont directement liées à l’inactivation du gène DDX17.
De manière complémentaire, une équipe de l’université de Portsmouth a réalisé un knock-out du gène DDX17 chez le crapaud xénope, un modèle animal particulièrement adapté à ce type de manipulation. Cette inactivation a révélé des anomalies similaires à celles observées chez la souris, notamment une croissance neuronale et axonale réduite.
De plus, une analyse comportementale des têtards dépourvus du gène a pu être réalisée. Grâce à des tests en labyrinthes, l’équipe anglaise a mis en évidence des altérations : alors que les têtards normaux alternent systématiquement entre les directions gauche et droite, ceux privés du gène DDX17 montrent un comportement désorganisé. Ces résultats traduisent une altération significative de leur mémoire de travail.
Bien qu’une comparaison directe avec les humains reste limitée, ces résultats renforcent l’hypothèse d’une implication du gène DDX17 dans les troubles du neurodéveloppement, accompagnée de répercussions comportementales.
En effet, le gène DDX17 est hautement conservé parmi les eucaryotes, c’est-à-dire qu’il est présent chez tous les organismes multicellulaires, depuis la levure jusqu’à l’humain. Cette conservation exceptionnelle tout au long de l’évolution met en évidence son importance biologique fondamentale.
Vers de nouvelles perspectives diagnostiques et thérapeutiques
Cette étude ouvre la voie à de nombreuses applications. « Notre objectif est d’inciter les cliniciens à intégrer le gène DDX17 dans leurs analyses génétiques afin d’identifier d’autres porteurs de mutations et de mieux comprendre les conséquences cliniques associées », souligne Cyril Bourgeois. À ce titre, une équipe néerlandaise gérant une base de données dédiée aux maladies génétiques rares (Human Disease Genes) a récemment pris contact avec lui afin de lui proposer d’être la personne référente pour le suivi et l’analyse des futurs cas cliniques identifiés. Cette plateforme permet de mettre en relation les familles de nouveaux patients avec des professionnels de santé et des chercheurs. D’un point de vue fondamental, les recherches futures viseront à décrypter les mécanismes par lesquels ces mutations altèrent la fonction de la protéine. De plus, plusieurs revues internationales ont mis en évidence le lien entre la famille de protéines à laquelle appartient DDX17 et les troubles du neurodéveloppement, ouvrant ainsi un champ d’investigation prometteur.
Une collaboration internationale exemplaire
Ce projet a impliqué quatre unités de recherche Inserm (Laboratoire de Biologie et Modélisation de la Cellule de Lyon, le laboratoire de Physiopathologie et Génétique du Neurone et du Muscle de Lyon, le Centre de Recherche en Cancérologie de Lyon, le laboratoire de Génétique des Anomalies du Développement de Dijon) et de nombreux partenaires à travers le monde. Il illustre la puissance de la science collaborative pour répondre à des questions complexes. La publication de ces travaux dans une revue prestigieuse souligne leur importance et leur potentiel impact pour les patients et les cliniciens.
Cette étude n’est qu’un premier pas dans l’exploration des rôles du gène DDX17 et ouvre la voie à des avancées significatives dans le diagnostic et la prise en charge des troubles du neurodéveloppement.
En résumé
En savoir plus:
Bonne nouvelle

A lire également
De la recherche fondamentale au patient, il n’y a parfois qu’un pas.
À l’occasion de la Journée Internationale des Maladies Rares, Thomas Boulin nous explique le lien entre troubles du neurodéveloppement, épilepsies sévères et le gène NBEA.
En savoir plus
Divercity : un dispositif pour améliorer l’inclusion dans la cité

Contexte
Depuis la loi de 2005 sur l’égalité des droits et des chances, les établissements recevant du public ont l’obligation de garantir leur accessibilité aux personnes en situation de handicap. Cependant, les aménagements actuels se concentrent principalement sur les handicaps moteurs ou sensoriels, tandis que les besoins liés aux handicaps invisibles — qui représentent 80 % des handicaps — sont souvent négligés. Les troubles du neurodéveloppement font partie de ces handicaps invisibles. Il en résulte un enjeu fort à favoriser activement l’inclusion de ces personnes dans la cité.
Cet enjeu est inscrit dans la Stratégie nationale 2023-2027 pour les troubles du neurodéveloppement : faciliter la vie des personnes, des familles et faire connaître les troubles du neurodéveloppement dans la société (engagement 6).
Objectif
L’objectif du projet Divercity est de créer un écosystème adapté aux particularités des personnes avec des troubles du neurodéveloppement, avec l’appui et le concours d’un réseau de lieux publics et de commerçants sensibilisés et répertoriés sur une application mobile participative. Ces aménagements seront également favorables à la qualité de vie des personnes vieillissantes, en situation de fragilité et plus globalement à l’ensemble de la population.
Le dispositif
L’inclusion dans la ville des personnes concernées par des troubles du neurodéveloppement nécessite que les lieux publics, de convivialité et les commerces puissent s’adapter à leurs particularités.
- L’application Divercity va permettre aux usagers et aux familles de géolocaliser, dans un premier temps dans la Métropole de Lyon, les commerces, lieux de convivialité, clubs de sport ou d’activités, proposant des aménagements adaptés.
- Ces établissements, sur la base du volontariat, bénéficieront d’une courte formation pratique en e-learning et signeront une charte d’engagement sur un ou plusieurs aménagements (spatiaux et fonctionnels).
Travaux préliminaires
Une enquête réalisée auprès de personnes avec des troubles du neurodéveloppement a été réalisée pour identifier les difficultés rencontrées et les aménagements souhaités.
Des capsules vidéo pour former les commerçants
Sur une plateforme dédiée, une série de 6 vidéos abordant les particularités des personnes concernées sont actuellement mises à disposition des commerçants souhaitant s’engager dans ce projet pour :
- Expliquer les difficultés rencontrées par ces personnes
- Indiquer quelques bonnes pratiques simples et peu coûteuses à mettre en place.
Ces vidéos portent sur les éléments suivants :
Elles sont également disponibles sur notre chaîne YouTube.
Une application construite de façon participative
Pour fournir la solution la plus juste, chaque étape du projet est réalisée avec la contribution de personnes concernées. Pour concevoir l’application, un groupe de travail composé de pair-aidants et de jeunes accompagnés par le SESSAD EVAI du pôle HU-ADIS du Vinatier – Psychiatrie Universitaire Lyon Métropole a ainsi travaillé sur trois aspects : le design graphique, l’expérience utilisateur et la rédaction des textes.
Au-delà du dispositif, un projet de recherche soutenu par Shape-Med@Lyon
L’application permettra de collecter des données acquises en situation réelle afin de mieux caractériser les comportements et préférences des usagers.
Un projet de recherche, en collaboration avec l’Université Lyon 2 et la participation du cabinet Mengrov, est en cours pour :
- Mesurer l’impact de l’application sur la qualité de vie des usagers
- Caractériser plus finement le comportement des usagers et mieux comprendre les préférences concernant les environnements bâtis
- Évaluer la pertinence des aménagements
- Rédiger un guide de bonnes pratiques pour la conception d’espaces
Par ailleurs, ce projet permettra également de :
- Mesurer l’impact de la sensibilisation et la perception des TND à moyen et long terme auprès des commerçants
- Évaluer les leviers et les obstacles pour la mise en place des aménagements
Un projet participatif
Le projet Divercity est impulsé par Le Vinatier, le Centre d’excellence iMIND et l’Institut des Sciences Cognitives Marc Jeannerod. Il bénéficie du soutien de la Fondation Orange et de Shape-Med@Lyon ainsi que du Synapse-Lab du Vinatier. Le projet de recherche est mené en collaboration avec l’Université Lumière Lyon 2 et avec la participation de l’agence de design sociétal Mengrov.
Des acteurs-clés sont mobilisés à chaque étape du projet :
- Conception des capsules vidéo et de l’application : groupe de travail (clinicien·nes, chercheurs et chercheuses, universitaires, représentant·es d’associations, pair-aidant·es, personnes concernées)
- Rédaction du cahier des charges de l’application : Le Vinatier (cellule innovation Digimentally et le Synapse Lab)
- Déploiement du dispositif et démarchage des différents lieux : commerces, équipements municipaux, lieux accueillant du public
- Recherche de soutien : collectivités territoriales, entreprises privées, fondations, associations d’intérêt public, particuliers

En résumé
- Une application utile pour les personnes concernées par l’autisme et les troubles du neurodéveloppement, et toute personne ayant des besoins spécifiques.
- Un projet pluridisciplinaire.
- Les personnes concernées impliquées à chaque étape du projet.
- Un projet de recherche innovant portant sur des données acquises en situation réelle.
Ce projet vous intéresse ?
Que vous soyez commerçant ou que vous travailliez dans un lieu accueillant du public, si vous souhaitez en savoir davantage sur le dispositif, nous vous invitons à renseigner vos coordonnées en consultant le site Divercity ou en nous envoyant un email.
Vous pouvez aussi suivre l’avancée du projet sur les réseaux sociaux : LinkedIn, Instagram et Facebook.
Liens utiles
- www.divercity.app
- Télécharger la plaquette de présentation de Divercity
- LOI n° 2005-102 du 11 février 2005 pour l’égalité des droits et des chances, la participation et la citoyenneté des personnes handicapées
- Nouvelle stratégie nationale pour les troubles du neurodéveloppement : autisme, Dys, TDAH, TDI
2023-2027
Annonce iMIND

A lire également
Divercity
Avec le dispositif Divercity, l’objectif est de créer un écosystème adapté aux particularités des personnes avec des troubles du neurodéveloppement, avec l’appui et le concours d’un réseau de lieux publics et de commerçants sensibilisés et répertoriés sur une application mobile participative.
En savoir plus
Conférence "Sérendipité et balle magique" par le Professeur Emmanuel FLAMAND-ROZE
La balle magique dessine le chemin suivi par les médecins-chercheurs : observation du monde, hypothèse, expériences … et découverte des remèdes. C’est souvent une utopie, une direction qui peut guider la quête du médecin-chercheur et enchanter son désir de trouver de nouveaux remèdes. Est-il cependant possible de la croiser par hasard dans un mouvement incertain de neurofantaisie ?
La sérendipité est-elle justement une version aléatoire de ce mouvement, un trait de poésie, la clochette d’une fée, la marque d’une intuition d’un esprit averti, ou encore une disposition d’esprit du médecin-chercheur ? quelle pourrait être la vertu de l’échec dans la rencontre de la sérendipité et de la balle magique ?
À partir d’anecdotes personnelles et de morceaux choisis, Emmanuel FLAMAND-ROZE (neurologue et chercheur) pose une lumière tendre ou critique sur le hasard de la découverte d’un traitement miraculeux pour les maladies orphelines du mouvement.
Biographie

Emmanuel FLAMAND-ROZE, M.D., Ph.D., est professeur de neurologie à Sorbonne Université à Paris et neurologue à l’hôpital de la Pitié-Salpêtrière.
Dans cet hôpital, il a développé un programme de soin de transition pour les adolescents et jeunes adultes avec des maladies neurologiques chroniques et a ensuite dirigé un consortium international pour l’élaboration de recommandations pour la transition dans le domaine des maladies du mouvement.
Il dirige une équipe de recherche à l’Institut du cerveau à Paris qui travaille sur les confins entre les troubles du mouvement et les troubles psychiatriques. Cette équipe a une dynamique translationnelle intégrant le travail sur des modèles cellulaires et animaux et des approches de recherche multimodale en physiopathologie humaine, pour aller vers la thérapeutique expérimentale.
Il a publié 335 articles, principalement sur la thématique des maladies du mouvement.
Enfin, il a beaucoup de goût pour l’enseignement et a développé un programme d’apprentissage de la neurologie à bas coût « The move », qui est largement utilisé dans de nombreuses universités dans le monde et dont l’efficacité a été largement démontrée.
Il est également le co-auteur d’un podcast sur le thème des humanités médicales qui est salué par le public et la critique, et dont l’efficacité pédagogique a également pu être démontrée (https://lesermentdaugusta.com). Il est depuis 3 ans le « chair » de la section pédiatrique de l’ « International Movement Disorders Society » et a co-créé un « virtual monthly videoround » afin de rendre accessible partout dans le monde l’enseignement de la connaissance autour des mouvements anormaux pédiatriques.
Informations pratiques
Date : jeudi 31 octobre 2024 de 15h30 à 17h00
Lieu : Amphithéâtre, bâtiment 416, 2e étage, Campus Hospitalier Le Vinatier, 95 boulevard Pinel, 69678 Bron
Conférence tout public
Participation gratuite sur inscription : yamina.lagha[at]ch-le-vinatier[dot]fr

Étude sur l’identité de genre dans l’autisme : appel à participation
Introduction
Une étude sur l’identité de genre chez les personnes présentant un Trouble du Spectre de l’Autisme (TSA) est lancée à l’automne 2024, sous la direction de Guilhem BONAZZI, psychiatre, et Élodie PEYROUX, neuropsychologue, du pôle hospitalo-universitaire ADIS (Autisme, neuroDéveloppement et Inclusion Sociale) du Vinatier – Psychiatrie Universitaire Lyon Métropole.
Cette étude a pour objectif d’accompagner au mieux les personnes autistes par rapport à cette question et de créer des ressources pour les professionnel·les accompagnant les personnes diverses de genre et les personnes autistes.

Critères d’inclusion
- Diagnostic de Trouble du Spectre de l’Autisme (TSA), validé par une équipe pluridisciplinaire ou un·e professionnel·le compétent·e
- Âge compris entre 18 et 60 ans, sans mesure de protection
- Sujet francophone maîtrisant la langue française (lue et parlée)
- Sujet affilié au régime de la Sécurité Sociale
- Pas de Trouble du Développement Intellectuel ou de trouble de la communication orale entravant la participation à l’étude
But de l’étude
Dans la littérature internationale, il apparait que les personnes concernées par un Trouble du Spectre de l’Autisme ont plus tendance que la population générale à avoir des intérêts, une apparence, un groupe d’amis, etc., en dehors des stéréotypes de genre habituels (Moore et al., 2022 ; Brunissen et al., 2021 ; Cooper et al., 2018 ; Cridland et al., 2014).
Le but de l’étude est de mieux comprendre le développement et la perception de l’identité de genre chez les personnes présentant un Trouble du Spectre de l’Autisme, pour les accompagner au mieux sur cette thématique.
Forme et durée de l’étude
La participation à cette étude se fera sous la forme d’un entretien individuel semi-dirigé, c’est-à-dire réalisé avec un guide d’entretien composé de questions préparées à l’avance, ce qui permettra de recueillir au mieux l’expérience des personnes.
Chaque entretien, d’une durée approximative d’une heure, permettra des échanges libres, avec la possibilité de faire des pauses si nécessaire. Le ou la participante sera seul·e avec la personne qui mènera l’entretien. L’entretien sera enregistré à l’aide d’un appareil d’enregistrement audio. Des notes seront prises lors de l’entretien puis l’enregistrement sera entièrement retranscrit.
Les témoignages seront anonymisés.
Informations pratiques
- Rémunération : 20 €/personne
- Lieu : Campus Hospitalier Le Vinatier 95 boulevard Pinel, Bron
- Date de début : 11 juillet 2024
- Télécharger l’appel à participation au format PDF : Appel_à_participation_Etude_genre_TSA
Comment participer ?
Les personnes intéressées par la participation à cette étude, et remplissant les critères, sont invitées à contacter :
- guilhem.bonazzi(at)ch-le-vinatier(dot)fr
- elodie.peyroux(at)ch-le-vinatier(dot)fr

Par Lucile Hertzog le 04/07/2024
Interview du Pr Pierre-Michel Llorca, président du comité scientifique des JNPN 2024
Le Pr Pierre-Michel Llorca est psychiatre et professeur des universités, exerçant au Centre Hospitalier Universitaire de Clermont-Ferrand. Spécialiste des troubles de l’humeur, il est une référence dans ce domaine.
Auteur de nombreuses publications scientifiques et reconnu pour son expertise, le Pr Llorca apporte une contribution majeure à l’avancée des connaissances et des pratiques cliniques dans la prise en charge des troubles psychiques.
iIl est le président du comité scientifique des Journées Neurosciences Psychiatrie et Neurologie (JNPN). C’est dans ce cadre que nous l’avons interrogé.

Quels sont les enjeux auxquels sont confrontés les domaines de la psychiatrie et de la neurologie aujourd’hui, et comment les JNPN tentent-elles d’y répondre ?
Aujourd’hui, nous travaillons en silo sur des pathologies très intriquées, comme les troubles neurologiques et les troubles psychiatriques. Cela altère la qualité de ce que l’on fait. Nous devenons spécialisés sur des sujets très précis, mais nous manquons de recul. Cela rend plus difficile le travail du point de vue purement clinique, de la recherche, et de la compréhension des troubles et des stratégies thérapeutiques en place.
Un des enjeux majeurs de la médecine, en tant que domaine hyperspécialisé, est de reconstruire une culture commune dans laquelle les neurosciences sont un véritable pont entre ces domaines cliniques qui ont longtemps été réunis.
Quel est l’intérêt d’une alliance entre psychiatrie et neurologie dans un contexte écologique et géopolitique de plus en plus tendu ?
La constatation c’est que le contexte écologique et géopolitique a des conséquences sur la santé mentale. Lorsque l’on pense par exemple aux liens bien connus entre l’alimentation, l’exposition environnementale (comme les pesticides), et certaines maladies neurologiques, tous ces éléments rendent indispensable l’amélioration de nos interactions entre les différentes disciplines.
Nous avons un réel besoin de nous préoccuper de l’identification des rôles de l’environnement dans les troubles psychiatriques et neurologiques, mais aussi dans des stratégies de prévention. Aux JNPN, vous rencontrerez au-delà des psychiatres et des neurologues, des professionnels de la santé publique, mais aussi des sciences humaines. Les chercheurs de ces domaines contribuent à la meilleure compréhension des risques.
Que pensez-vous du décalage existant entre la recherche aux Etats-Unis et en Europe, notamment dans leur approche dimensionnelle ou catégorielle ?
C’est une question importante… Je ne suis pas certain qu’il y ait une avance ou un retard, mais je suis conscient de l’existence d’un décalage. Il a un intérêt puisque aujourd’hui, nous parvenons à avoir en France le développement de programmes moins dogmatiques que ce qui a été fait aux Etats-Unis il y a une dizaine d’années, avec les RDoC pour appréhender l’articulation dimension-catégorie, en créant une matrice basée sur des construits psychologiques et leur niveau d’étude allant du gène au comportement.
Peut-être que cela a été un bon moyen de prendre un peu de recul par rapport aux classifications “classiques” (ICD ou DSM). Saura-t-on bénéficier de ce recul pour ne pas faire les mêmes erreurs ? Je ne sais pas. On peut s’y employer, mais je ne suis pas sûr que l’on arrive à dépasser la rigidité de nos modalités de réflexion.
Le côté dogmatique des RDoC vient de l’ambition initiale de remplacer les classifications catégorielles, mais en réalité c’est plutôt une matrice qui permet la réflexion surtout de caractériser les projets de recherche, ce qui n’est pas la même chose. Le côté extrêmement rigide de cette matrice fait que tous les troubles ou tous les projets de recherche ne peuvent pas “passer à la moulinette” des Rdoc. Cela a servi aux Etats-Unis à structurer les financements des projets de recherche. Et ça, c’est un problème très américain qui n’est pas le nôtre.
Quelles sont les avancées scientifiques récentes les plus prometteuses en psychiatrie et en neurologie ?
En psychiatrie, les avancées sur l’utilisation des psychédéliques par exemple, sont assez intéressantes d’un point de vue sociologique, puisque l’on est passé de drogues récréatives pour “ouvrir l’esprit” qui étaient bannies du champ de la recherche, à des outils majeurs de l’innovation pharmacologique. Cela permet de réelles innovations, mais pose un certain nombre de problèmes de mise en œuvre. Cette évolution que je trouve très prometteuse, issue d’un long chemin assez intéressant, permettra, je l’espère, des bénéfices pour les patients à court terme.
En neurologie, je retiens deux choses.
D’une part, la conférence du Pr Duffaut sur la neurochirurgie éveillée, et la manière de prendre en compte la connectomique comme un outil de préservation fonctionnelle dans des pathologies neuro-oncologiques sévères. C’est tout à fait remarquable et cela reste peu connu. L’enjeu est que cela devienne accessible au plus grand nombre.
D’autre part, tout ce qui a été évoqué sur les perspectives concernant la maladie d’Alzheimer, avec notamment des nouvelles stratégies thérapeutiques. Elles ne stoppent pas l’évolution de cette maladie dégénérative, mais il y a des enjeux fonctionnels majeurs pour les patients, après de nombreuses promesses non abouties dans ce champ de recherche.
Au cours des JNPN, de nombreuses pistes de recherche ont été présentées, sur de nombreux sujets. Je viens d’évoquer les résultats qui sont à court terme, potentiellement d’intérêt pour les patients. Mais il y a beaucoup, beaucoup de choses qui, dans deux ans, cinq ans, dix ans, seront probablement des outils de demain.
Quelle place occupe la prévention dans les réflexions menées lors des JNPN, que ce soit en termes de facteurs de risque ou de dépistage précoce ?
Dans l’aspect santé publique, nous avons eu une session spécifique sur un concept développé aux Etats-Unis. Il a un enjeu réel concernant la santé des soignants : c’est la notion de “blessure morale” (moral injury). Elle permet de ne pas résumer les difficultés des soignants au “simple burn-out” en ne mettant pas l’accent sur la vulnérabilité individuelle des soignants, mais plutôt sur le rôle de pratiques systémiques soignantes entraînant des conflits de valeurs chez les professionnels, et une souffrance du fait de ces conflits. C’est probablement une des causes de la désaffection des soignants. Identifier des causes à de telles situations de santé publique, cela permettrait de développer des stratégies préventives. L’idée est de pouvoir se saisir de ces enjeux pour essayer de promouvoir cela en Europe, et de mesurer sa pertinence. Cela pourrait-il nous permettre des changements qui auront une action préventive ? Il ne s’agit plus de se centrer sur les soignants uniquement. Cela concerne tout de même la désaffection des professionnels pour les métiers du soin, et c’est une vraie question dans une telle société.
Quels sont les défis spécifiques liés à la prise en charge des troubles psychiatriques résistants aux traitements conventionnels ?
La prise en charge spécifique, c’est à mon avis l’un des enjeux immédiats. Le principal problème de la résistance, passe par une amélioration de l’identification et des pratiques qui permettent de les éviter. C’est un premier enjeu de modification des pratiques.
Le deuxième enjeu : l’exploration physiopathologique de ces patients résistants sont des outils qui sont des situations à fort enjeu, pour trouver des stratégies pertinentes pour ses patients. À l’heure actuelle, cela se fait souvent de manière incrémentale, en modifiant des traitements, en les associant avec des petits progrès, mais qui sont non négligeables. Et de l’autre côté, c’est la compréhension physiopathie des troubles en eux-mêmes et la modification des stratégies.
Nous remercions chaleureusement le Pr Pierre-Michel Llorca de nous avoir accordé de son temps.
Retrouvez le résumé d’une partie des conférences sur notre compte LinkedIn ainsi que le replay de la journée :
- Le consentement : aspects neuroscientifique clinique et juridique →
- Comment sont guidés nos choix →
- Les enjeux de la recherche pharmacologique en psychiatrie →
- La représentation de soi et de l’autre à travers le toucher →
- La psychiatrie de précision, ici et ailleurs →
- La notion de « moral injury » : quels enjeux de santé publique →
- Addictions et sport : le cerveau joue les prolongations →
- Genopsy : maladies rares →
- Amnésie dissociative →
- Épistémologie partout →
Newsletter

04/10/21, par Jennifer Beneyton
Nouvelle publication iMIND dans Molecular Psychiatry
Présentation
L’amélioration de la qualité de vie des personnes avec des troubles du neurodéveloppement reste au coeur des préoccupations de l’hôpital du Vinatier, de l’Institut des Sciences Cognitives Marc Jeannerod et du Centre d’Excellence iMIND. Pour ce faire, il est urgent d’améliorer la démarche diagnostique, le repérage précoce et la compréhension des mécanismes biologiques impliqués. Une équipe de chercheurs·es Vinatier/iMIND, sous l’impulsion de la Professeure Caroline Demily, explore une piste prometteuse dans ce domaine en se concentrant sur les interactions entre le corps et le cerveau. En effet, la recherche sur les troubles du neurodéveloppement dont l’autisme se concentre largement sur le cerveau. Or, comme le cerveau interagit de façon continue avec le reste du corps, l’étude des interactions entre le cerveau et d’autres organes, comme les intestins et la peau, semble particulièrement intéressante. Cette hypothèse de recherche, acceptée dans la revue universitaire internationale Molecular Psychiatry appartenant au prestigieux groupe d’édition Nature Publishing, examine le potentiel de l’imagerie cellulaire en 3D par microscopie à feuilles de lumière pour étudier la biologie du développement et la connectivité le cerveau et d’autres organes périphériques, offrant ainsi de nouvelles perspectives pour une prise en charge davantage personnalisée.
Publication
Soumier A, Lio G, Demily C (2024) Current and future applications of light-sheet imaging for identifying molecular and developmental processes in autism spectrum disorders, Molecular Psychiatry.
Lien vers l’article : https://www.nature.com/articles/s41380-024-02487-8
Newsletter

SenseToKnow: vers un dépistage de l'autisme précoce et automatisé?

Une étude récente publiée dans Nature Medicine relate les résultats remarquables d’une nouvelle application, nommée SenseToKnow (S2K), dans le dépistage précoce de l’autisme. Cette application a été créée par des chercheurs·es de l’université Duke en partenariat avec le Centre Borelli à Paris. Sam Perochon, l’un des principaux auteurs de l’étude, a accepté de répondre à nos questions.
Pouvez-vous nous expliquer la genèse du projet ?
Cette application est le fruit d’une collaboration de longue date entre Geraldine Dawson, directrice de recherche en psychologie du développement, spécialisée dans l’autisme à Duke University, et Guillermo Sapiro, directeur de recherche en mathématiques appliquées au sein de l’université de Duke, avec qui j’ai fait un stage de 10 mois pendant mon cursus à l’ENS Paris-Saclay. C’est passionné par le sujet que j’en ai fait mon sujet de thèse, que j’effectue aujourd’hui à cheval entre le Centre Borelli et Duke. La Dre Geraldine Dawson et son équipe ont apportés toute l’expertise clinique, travaillant en étroite collaboration avec des personnes concernées et des psychiatres, tandis que le Dr Sapiro, son équipe et moi-même avons développé des algorithmes pour analyser les données récoltées. Cet article est un aboutissement dans le sens où il compile tous les marqueurs comportementaux mis en évidence ces dix dernières années et sur lesquels sont basés les différents modules constitutifs de l’appli. L’intérêt de cette étude et de cette application, réside dans le fait qu’elles couvrent un large spectre de marqueurs comportementaux reliés à l’autisme, permettant ainsi de couvrir une grande partie de la complexité des manifestations individuelles de l’autisme chez les individus concernés.
Comment fonctionne l’application ?
L’application se compose de 10 vidéos très courtes, d’une durée de 30 à 45 secondes chacune, et d’un petit jeu appelant les enfants à interagir avec l’écran. Chaque composante a été pensée autour d’une hypothèse de recherche basée sur l’état de la littérature concernant les manifestations comportementales précoces de l’autisme. Cela permet de mettre en évidence chez les utilisateurs·rices de l’application, des marqueurs comportementaux de l’autisme que nous avons validé années après années, en lien avec le regard, les micro-expressions faciales, les clignements d’yeux, les mouvements de la tête, le contrôle moteur et l’intégration visuelle d’information, la réponse à l’appel du prénom, etc… Par exemple, certains marqueurs se basent sur l’extraction de 49 points d’intérêt sur le visage, et s’intéressent à la complexité des micro-expressions associées aux mouvements de la bouche et des sourcils, en particulier pendant les vidéos à caractère social ou non-social.

Nos recherches ont permis de montrer qu’il était possible de reproduire ou d’adapter des tests connus de la littérature, pour diagnostiquer l’autisme, mais aussi de révéler de nouveaux marqueurs grâce à des avancées technologiques permettant des mesures beaucoup plus fines et précises. C’est le cas de la mesure du temps de réponse à l’appel du prénom, ou de la mesure de la synchronisation entre le regard de l’enfant et la personne qui parle dans les vidéos. Chez les individus neurotypiques par exemple, on observe une anticipation du regard plus prononcée vers la personne qui s ‘apprête à parler, une caractéristique moins marquée chez les personnes autistes.
Quelles sont les conditions d’administration de l’appli ?
L’ensemble des données de notre étude, comprenant 475 sujets, a été collecté dans 4 centres de recherche en Caroline du Nord. Les familles participent volontairement à l’étude lors d’une visite médicale de routine non obligatoire pour les enfants âgés de 18 à 24 mois (appelée well-child visit aux Etats-Unis). La prévalence du TSA dans cette étude, dépassant les 10% par rapport aux 2% observés dans la population générale, indique que les familles se présentant dans ces centres se questionnent sur une éventuelle atypicité développementale de leur enfant. Le test dure une douzaine de minutes. L’enfant est assis sur les genoux de son parent. En début de session, une vidéo sert au calibrage automatique du regard, affinant l’estimation des coordonnées X (axe horizontal) et Y (axe vertical) du regard de l’enfant sur l’écran. À la fin de l’administration de l’appli, un petit jeu ludique est présenté à l’enfant pour évaluer sa motricité fine. Les conditions d’administration visent à favoriser un environnement non contraignant où l’enfant n’est en aucun cas forcé de regarder la vidéo. Notre intention est de permettre l’expression libre des saillances comportementales liées aux traits autistiques.

D’un point de vue technique, comment enregistrez-vous le regard ?
L’enregistrement s’effectue via la caméra frontale de l’iPad qui sert également de support de l’application. Dans une première phase, le développement d’algorithmes était nécessaire pour identifier la personne d’intérêt dans les enregistrements, notamment lorsque plusieurs personnes apparaissent à l’écran, comme le parent accompagnant ou d’autres frères et sœurs. Ensuite, nous avons utilisé des algorithmes pour estimer avec précision le regard simplement à partir des enregistrements. Nous sommes aussi très vigilants avec la qualité des vidéos pour être sûr qu’elles soient bien conformes à notre protocole. Nous avons donc établi un indicateur de qualité des conditions d’administration, qui comprend des paramètres tels que la proportion du visage de l’enfant dans la vidéo qui doit être suffisamment grande ou une luminosité suffisante. Il est à noter que les performances de l’estimation sont généralement meilleures pour les coordonnées X que pour les coordonnées Y. Cela dit, tous les marqueurs ne sont pas exclusivement liés au regard. C’est aussi ce qui fait la force de cette application. Les marqueurs comportementaux, basés sur le regard, représentent seulement l’une des composantes de cette application.
À votre avis, est-ce que cette application serait en mesure de mieux dépister l’autisme que les professionnels ?
Je trouve que l’idée d’explorer des moyens standardisés que permettent l’utilisation d’algorithmes ou la technologie en général, pour réduire les biais de subjectivité dans les dépistages actuels est vraiment intéressante. Cela apporterait une certaine objectivité aux processus de détection. Cependant, dire que cela pourrait remplacer à terme le travail des professionnels·les me semble très peu probable. L’objectif de ces travaux est plutôt d’automatiser certaines tâches réalisées dans le cadre du dépistage de l’autisme. Des comparaisons de performances entre les tests de dépistage existants et l’application doivent guider cette réponse. Je pense avant tout que cette approche offre l’avantage de rendre le dépistage beaucoup plus accessible et rapide, ce qui constitue un progrès significatif.
Avez-vous eu des faux positifs ?
Les performances sont remarquables : l’appli a réussi à reconnaître 87,8 % des enfants autistes et 80,8 % des enfants non autistes, et 40,6 % des enfants identifiés par l’appli comme présentant des traits autistiques ont par la suite fait l’objet d’un diagnostic clinique d’autisme. Il subsiste donc toujours des cas de faux positifs, qui s’expliquent notamment par l’hétérogénéité des phénotypes comportementaux liés à l’autisme. Certains enfants présentent des comportements qui sont à la fois très neurotypiques sur certaines caractéristiques et très autistiques sur d’autres.
Enfin, l’une des exigences du projet est de pouvoir donner une explication sur la prédiction faite par l’appli. Cette explication prend la forme d’un phénotype comportemental associé à la détection, qui indique parmi les variables de l’appli celles qui ont été importantes pour établir la prédiction. Il est important de souligner que les tests ne sont en aucun cas parfaits, et nous ne disposons d’aucun marqueur véritablement prédictif. L’application vise à saisir des saillances comportementales diverses en lien avec l’autisme. Une perspective envisageable pourrait être de poursuivre le développement de marqueurs comportementaux associés à cette application, relatifs aux vocalisations de l’enfant, au degré d’attention jointe avec le parent, ou aux évènements de pointage souvent observés. Cependant, il convient de reconnaître les limitations importantes de cette approche. Étant donné l’hétérogénéité des manifestations symptomatiques de l’autisme, certaines facettes sont difficiles à imaginer capturer avec une application de ce type, comme celles liées à l’acquisition du langage ou aux comportement répétitifs.

Quelle est la prochaine étape pour cette appli ?
Avec le COVID, nous avons développé un protocole permettant aux familles d’administrer l’application à leur enfant au sein de leur foyer. Les premiers résultats semblent indiquer que la fiabilité de l’application reste constante malgré les différences structurelles observées. On constate, par exemple, une grande diversité des appareils utilisés (téléphone, tablette, ordinateur, etc.). Nous essayons donc de voir si la taille de l’écran exerce une influence sur la qualité de la calibration du regard et donc des résultats. Il est aussi important de noter que, contrairement à notre installation habituelle avec une tablette sur un trépied, les familles placent souvent leurs téléphones sur une table, ce qui peut réduire la détection des oscillations dynamiques du dispositif qui sont utiles pour capturer la force avec laquelle les enfants tapent sur l’écran quand il est posé. Cela peut donc altérer la fiabilité des marqueurs liés au contrôle moteur.
En outre, actuellement, les familles ne sont pas totalement autonomes dans l’utilisation de l’application. À chaque session, un assistant de recherche se connecte via Zoom pour superviser le déroulement de l’expérience et recueillir des informations précieuses sur la manière dont s’est passée l’administration de l’application.
Pour faciliter la mise en place pour les familles, nous avons créé une chaîne YT qui héberge des vidéos simples et claires, en anglais et en espagnol, permettant d’expliquer aux parents et aux enfants le fonctionnement de l’application et son objectif. Nous avons également défini des critères pour évaluer la qualité de l’administration et déterminer si une réadministration est nécessaire.
Une fois que les performances de l’appli à domicile auront été validées dans le cadre d’une étude clinique sur une large cohorte, alors, nous envisagerons de passer à l’étape de diffusion massive de l’application.
Pour aller plus loin
- Chaîne Youtube SenseToKnow
- Publication dans Nature Medecine
- Validation de la mesure du regard
- Validation de l’analyse des micro-expressions faciales
- Validation de l’analyse des mouvements de la tête
- Validation du test de l’appel du prénom
- Validation de l’analyse de l’orientation de la tête et des clignements
- Validation des variables de motricité et d’intégration visuelle
- Relation entre les variables de l’appli et le profil clinique des enfants

Nous avons besoin de vous pour une étude sur la prise en charge en remédiation cognitive !
Contexte
Les adultes avec une déficience intellectuelle ont des difficultés pour s’adapter aux situations sociales, ce qui peut générer des troubles du comportement. Les troubles cognitifs sont un des facteurs permettant de comprendre ces difficultés. Dans le domaine de la reconnaissance des émotions faciales, les capacités attentionnelles et visuo-spatiales sont fortement impliquées.
Objectifs
Montrer l’efficacité du programme de remédiation cognitive « REHABILITUS » chez des adultes de 18 à 45 ans présentant une déficience intellectuelle légère à modérée et des troubles du comportement associés
Profils
Eloïse MASOERO, neuropsychologue, souhaite recruter des adultes de 18 à 45 ans présentant une déficience intellectuelle légère à modérée et des troubles du comportement associés.
Déroulement
1 – Première évaluation afin de connaitre les points forts et les faiblesses.
2 – 1 séance de psychoéducation + 16 semaines de prise en charge (1 séance /semaine)
Les participants seront placés dans un groupe « REHABILITUS » ou dans un groupe « Contrôle ». La répartition sera faite par un tirage au sort aléatoire.
3 – Deuxième évaluation afin d’observer les améliorations.
4 – Pause de 6 mois
5 – Troisième et dernière évaluation afin vérifier le maintien des progrès.
Une fois l’étude terminée, les sujets du groupe contrôle pourront bénéficier du programme « REHABILITUS ».
Contact
- Pour participer ou poser vos questions, contactez Eloïse MASOERO
- Lieu de l’étude : CH le Vinatier, Unité GénoPsy (bâtiment 505), 95 Bd Pinel, 69500 BRON
- Télécharger le flyer de l’étude
Newsletter

On a besoin de vous pour une étude sur le jugement moral!
Contexte
Le jugement moral permet de caractériser, du point de vue d’un individu, ce qui est bien ou mal. A l’heure actuelle, il est admis que, relativement aux personnes neurotypiques, les personnes avec un Trouble du Spectre de l’Autisme (TSA) présentent des schémas de jugements moraux marqués par une minimisation de l’intentionnalité et une forte condamnation des agents responsables d’accidents.
Objectifs
Etudier la manière dont les personnes avec TSA assignent des émotions à différentes formes d’offense morale et examiner si leurs performances contrastent avec celles des neurotypiques.
Profils
Elodie Peyroux neuropsychologue du pôle HU-ADIS et Romane Chazelle, souhaitent recruter des adultes porteurs d’un TSA sans trouble du développement intellectuel et des adultes neurotypiques âgés de 18 à 40 ans. Les participants recevront un forfait transport à hauteur de 30€.
Déroulement
L’étude se déroule en 2 rdv d’1h30 et propose :
- La passation de tests neuropsychologiques
- Un protocole expérimental constitué de vignettes présentant des transgressions morales
Contact
- Pour participer ou poser vos questions, contactez Romane CHAZELLE: romane[dot]chazelle[at]ch-le-vinatier[dot]fr
- Lieu de l’étude : Pôle Hospitalo-Universitaire ADIS, CH Le Vinatier, 95 bd Pinel BP 30039 69678 BRON Cedex
- Télécharger le Flyer CoMorA de l’étude

Lancement de la Cohorte MARIANNE
Le projet de cohorte MARIANNE a été lancé officiellement le mercredi 29 mars à l’occasion d’une inauguration par Mme Geneviève DARRIEUSSECQ, Ministre déléguée aux personnes handicapées.
Un programme de recherche national intitulé MARIANNE va suivre 1 700 familles pour étudier les effets conjugués des facteurs génétiques et environnementaux dans l’apparition de l’autisme et autres difficultés de développement chez l’enfant (langage, motricité, attention, par exemple).
Deux membres d’iMIND y participent: Sandrine Sonié (CRA) et Julien Dubreucq (CHU Saint-Etienne).
Qui peut participer ?
Les femmes enceintes, majeures, déjà maman, dans l’une des situations suivantes :
- Elles (ou le futur papa) ont un enfant autiste
- Elles (ou le futur papa) ont des enfants dont aucun n’a de trouble du développement
- Elles résident dans les départements suivants :
Eure, Gard, Haute-Garonne, Hérault, Nord, Loire, Tarn, Tarn et Garonne, Rhône, Seine-Maritime.
Comment se déroule l’étude ?
Un suivi est proposé à partir du deuxième trimestre de grossesse et jusqu’aux 6 ans de l’enfant. Il comporte des rendez-vous réguliers des familles avec des professionnels comme des sages-femmes et des psychologues dans des centres participants proches de chez elles. Le suivi comportera également des questionnaires, et si les familles l’acceptent, des prélèvements biologiques, mèches de cheveux et urines par exemple. Le suivi lié à l’étude est entièrement pris en charge.
Pourquoi participer ?
Les familles bénéficieront de l’écoute attentive et de conseils personnalisés de professionnels tout au long du suivi. Par leur participation, elles aideront à mieux comprendre les déterminants des troubles du neuro-développement et comment améliorer la santé des enfants.
Qui conduit l’étude ?
L’étude MARIANNE est menée en collaboration entre plusieurs hôpitaux universitaires (Montpellier, Toulouse, Saint-Etienne, Lille, Lyon et Rouen), des maternités et l’INSERM (Institut national de la santé et de la recherche médicale). MARIANNE est soutenue par les Caisses d’Assurance Maladie, les Caisses de Mutualité Sociale Agricole et les Caisses d’Allocations familiales.
Contact
Les familles qui souhaitent participer ou avoir des informations peuvent :
- téléphoner au 04 67 33 85 39
- écrire à contact-marianne@chu-montpellier.fr

Le pari de la recherche participative : créer un dialogue équitable entre personnes autistes et chercheur.es

Présentation
À l’heure où les financements se font plus rares, il devient primordial que les organismes de recherche inscrivent leurs projets dans des problématiques portées par la société civile et en particulier par les associations de patients dont les attentes sont fortes. Cette nouvelle méthodologie nécessite de lever certains freins, de part et d’autre, pour permettre un dialogue fructueux. Nos deux intervenants partageront leurs points de vue et leurs expériences sur la question.
Les intervenants
- Josef Schovanec, philosophe, écrivain et personne concernée par un trouble du spectre de l’autisme nous livrera son savoir expérientiel dans la recherche participative.
- Stanislas Lyonnet, professeur de Génétique à la Faculté de médecine Paris Descartes et généticien de l’hôpital universitaire Necker-Enfants Malades à Paris, présentera la façon dont il a impulsé une dynamique de recherche participative au sein de l’institut Imagine qu’il dirige.
Cet évènement était organisé dans le cadre du colloque Neurofrance avec le soutien de la Ville de Lyon et animé par Caroline Demily, chef du pôle HU-ADIS du Centre Hospitalier Le Vinatier et coordinatrice du centre d’excellence iMIND.
Replay

Le pari de la recherche participative : instaurer un dialogue avec les personnes concernées

Présentation
Que chacun.e puisse accéder à une bonne compréhension de la science en général et de la recherche fondamentale en particulier est essentiel pour la société comme pour les citoyens. Aujourd’hui, un changement de paradigme pousse les chercheur.es à ouvrir leurs laboratoires au grand public et à montrer ce qu’ils étudient, pourquoi le faire, comment ils s’y prennent… Intégrer le plus possible les personnes concernées dans toutes les phases du processus est aussi l’un des nouveaux objectifs. Cette collaboration, du fait de sa nouveauté, nécessite des explications et des ajustements, et donc une construction commune.
Dans ce webinaire, nous avons invité Amélie Soumier, chercheure en neurosciences et Danièle Langloys, présidente d’association, pour les entendre sur leurs attentes respectives, leurs points de vue et sur des pistes qu’elles ont identifiées pour permettre un dialogue fructueux.
Les intervenants
- Amélie Soumier, chercheure en neurobiologie cellulaire et moléculaire, s’intéresse aux réseaux de l’ocytocine fortement suspectés comme étant impliqués dans l’apparition des troubles du spectre autistique grâce à une approche innovante d’imagerie cellulaire qui permet de cartographier le développement cérébral.
- Danièle Langloys est la présidente de l’association Autisme France.
Replay disponible :

De la recherche fondamentale au patient, il n’y a parfois qu’un pas.
Thomas Boulin, chercheur au CNRS et directeur de l’équipe « Neurobiologie moléculaire et cellulaire de C. elegans » du laboratoire MeLiS, a réalisé une partie des tests de validation diagnostique qui a permis à un organisme américain, l’UDN, d’identifier l’origine génétique des troubles du neuro-développement (TND) d’une jeune patiente, le syndrome NEDEGE qui résulte d’une mutation du gène NBEA. Lui qui d’habitude se passionne pour des questions de recherche fondamentale, a éprouvé un regain d’enthousiasme à pouvoir appliquer sa recherche pour confirmer le diagnostic d’une jeune patiente américaine.

« La recherche, ce n’est pas un chercheur qui se lève le matin en décidant d’étudier une pathologie pour savoir comment elle fonctionne. Ça ne se passe pas comme ça, sinon, on n’aurait plus de cancer ».
C’est avec ces mots que Thomas Boulin a commencé son récit. En effet, la recherche scientifique reste un mystère pour beaucoup. On distingue la recherche fondamentale, qui vise à comprendre les phénomènes biologiques et dont le but est le progrès de la connaissance, à laquelle on oppose souvent, de façon erronée, la recherche appliquée dont le but est de répondre à une question précise, par exemple clinique. Alors que le financement de la recherche se fait aujourd’hui essentiellement par appels d’offres ciblés, la recherche fondamentale est davantage critiquée sur son utilité, en comparaison à la recherche appliquée, plus concrète à première vue. Or, sans recherche fondamentale, pas de recherche appliquée car celle-ci s’appuie sur le socle de connaissance issu de la recherche fondamentale. L’équipe de Thomas Boulin du laboratoire MeLiS étudie le fonctionnement des canaux potassiques qui régulent l’activité électriques des neurones. En d’autres termes, il cherche à comprendre les conditions nécessaires, au niveau moléculaire, pour que l’information circule correctement dans nos réseaux neuronaux. Ses travaux se situent donc dans le champ de la recherche fondamentale. C’est pourtant grâce à ces travaux qu’il a pu développer un nouvel outil diagnostic pour le syndrome NEDEGE.
Le parcours diagnostic dans les maladies rares
Beaucoup de maladies rares ont une origine génétique. Le parcours patient classique consiste à faire des examens génétiques pour identifier des gènes-candidats, c’est-à-dire des gènes comportant une mutation qui pourrait être à l’origine de la maladie rare. En plus du génome du patient, on séquence donc le génome des parents car ces mutations apparaissent fréquemment après la fertilisation de l’ovocyte par un accident génétique lors de la reproduction de l’ADN. On dit qu’il s’agit de « mutations de novo ». Aucun des deux parents n’ayant la mutation, la comparaison du génome des parents et de l’enfant permet d’identifier cette liste de gènes-candidats. Souvent, le parcours médical s’arrête là car les médecins n’ont pas forcément les savoirs, ni les outils technologiques pour aller plus loin. C’est là qu’entre en scène Hugo Bellen, un généticien de la mouche Drosophile et son réseau américain, UDN, Undiagnosed Diseases Network, dont l’originalité est de mettre des plateformes technologiques de pointe au service du diagnostic génétique et de démontrer qu’une mutation est bien à l’origine de la maladie du patient.
Qu’est-ce que l’UDN?
 L’UDN, pour Undiagnosed Diseases Network, est un réseau américain de quatorze sites universitaires et hospitaliers les plus prestigieux du pays, financé par le NIH. Un patient, ou sa famille, en errance diagnostique peut déposer auprès de cet organisme un dossier composé de tous ses antécédents et tests médicaux. Pour les patients pris en charge, l’UDN étudie tous les éléments du dossier et va actualiser certains tests ou faire des tests complémentaires, à la lumière des avancées technologiques et scientifiques les plus récentes. C’est entièrement pris en charge par le réseau, ce qui n’est pas négligeable lorsqu’on connaît le coût des frais médicaux aux États-Unis.
L’UDN, pour Undiagnosed Diseases Network, est un réseau américain de quatorze sites universitaires et hospitaliers les plus prestigieux du pays, financé par le NIH. Un patient, ou sa famille, en errance diagnostique peut déposer auprès de cet organisme un dossier composé de tous ses antécédents et tests médicaux. Pour les patients pris en charge, l’UDN étudie tous les éléments du dossier et va actualiser certains tests ou faire des tests complémentaires, à la lumière des avancées technologiques et scientifiques les plus récentes. C’est entièrement pris en charge par le réseau, ce qui n’est pas négligeable lorsqu’on connaît le coût des frais médicaux aux États-Unis.
Dossier UDN N°068
Bien que doté de moyens très importants, ce réseau s’appuie aussi sur l’expertise de collaborateurs internationaux et lance régulièrement des appels à la communauté scientifique. C’est ainsi qu’un jour apparaît sur ce portail le cas d’une jeune fille américaine porteuse d’un trouble du neuro-développement sévère avec un trouble du développement intellectuel et des crises d’épilepsie fréquentes pour laquelle l’UDN a identifié le gène Neurobeachin (NBEA) comme gène-candidat principal. En effet, une étude de 2019 très récente avait montré un lien entre les troubles du neuro-développement, l’épilepsie et ce gène. Quand Thomas voit cet appel, ça fait tilt !
Il se trouve que Sonia El Mouridi, doctorante dans l’équipe, avait découvert un rôle nouveau de la Neurobeachin dans les processus biologiques qui intéressent l’équipe. N’étant pas le cœur de son projet de doctorat, cette observation était simplement présentée dans une annexe de sa thèse sans avoir été formellement publiée. Qui aurait pu prédire que, quelques années plus tard, forte de ces résultats et de son expertise sur le ver C. elegans, l’équipe de Thomas allait pouvoir réaliser pour l’UDN une partie des tests de validation fonctionnelle démontrant que cette mutation inconnue jusque-là était bien à l’origine des troubles de la patiente et aider ainsi à confirmer le diagnostic génétique de la maladie rare de cette jeune fille.
Comment l’équipe s’y est-elle prise ?
Un modèle animal sur mesure
Pour démontrer l’effet délétère d’une mutation identifiée chez un patient, il est très souvent nécessaire de passer par des modèles animaux. La souris serait tout à fait pertinente mais cela reste extrêmement cher et long et surtout, impossible à réaliser à grande échelle. L’approche préconisée par l’UDN et Thomas Boulin s’oriente donc vers des modèles animaux plus simples, moins coûteux et où le temps de génération est plus rapide. Ainsi la drosophile, le poisson zèbre, mais aussi le ver C. elegans sont des modèles de choix. On est en droit de se demander en quoi la drosophile ou le ver C. elegans sont des modèles pertinents pour étudier l’humain étant donné que nous n’avons pas grand-chose en commun à première vue. Il s’avère en réalité, que notre patrimoine génétique n’est pas si différent. Les gènes affectés dans les maladies rares sont souvent des gènes très importants, maintenus au cours de l’évolution, et que l’on retrouve chez l’humain, mais aussi chez la drosophile ou le ver C. elegans. C’est ce qu’on appelle la conservation évolutive.
Qu’est-ce que C. elegans ?
Le nématode C. elegans est un ver d’un millimètre de long, à peine visible à l’œil nu. Il est l’un des modèles animaux utilisés en biologie depuis 50 ans pour disséquer les processus biologiques fondamentaux, comme par exemple la mort cellulaire programmée qui est impliquée dans le cancer. Cet « organisme modèle pionnier » est très prisé pour les études génétiques du fait de sa robustesse, de son temps de génération extrêmement rapide (3 jours), des nombreux outils génétiques disponibles et de son coût très limité.
La révolution CRISPR-Cas9
Récapitulons : nous avons une patiente, un gène candidat, NBEA, et un modèle animal, le ver C. elegans, spécialité de l’équipe de Thomas. La première étape a donc consisté à reproduire la mutation identifiée chez la patiente dans le génome de C. elegans afin de créer un « modèle sur mesure ». Grâce à la technologie des « ciseaux moléculaires » CRISPR-Cas9, on peut aujourd’hui d’introduire une cassure dans un gène cible afin de forcer la cellule à la réparer avec une séquence génétique artificielle, contenant la mutation. Avant de mettre au point cette technologie, on avait tendance à surexprimer les protéines mutées, ce qui a souvent des effets délétères et peut entraîner des artefacts. L’approche CRISPR-Cas9 permet maintenant de faire des modifications génétiques de façon très fine, sans modifier ce qu’il y a autour. On peut ainsi étudier l’impact d’une mutation dans un modèle animal de la façon la plus fidèle possible.
La validation de mutation
La Neurobeachin est une protéine immense composée de 2500 lettres, ou acides aminés. Or, la mutation de la patiente n’affecte qu’un seul de ces acides aminés, et ce, en opérant un simple remplacement par un autre acide aminé. Or les dysfonctionnements produits par ce type de substitutions sont presque impossibles à prédire théoriquement. Grâce aux animaux génétiquement modifiés, Thomas et son équipe ont donc procédé à différents tests fonctionnels pour vérifier l’impact de la mutation sur le fonctionnement de la Neurobeachin. Grâce à ces tests, l’UDN a été en mesure de conclure avec certitude que cette mutation sur le gène NBEA de la patiente était bien à l’origine de sa maladie rare.
De l’importance d’identifier ces syndromes
Valider l’impact d’une mutation et mettre un nom sur un syndrome permet d’apporter la certitude au patient, à ses proches et à l’équipe médicale que la pathologie est bien liée à la mutation d’un gène. L’errance diagnostique prend fin, ce qui représente souvent un grand soulagement psychologique pour la famille. Une fois que le diagnostic a été posé, les personnes concernées par ce syndrome peuvent se rencontrer : d’une part pour échanger sur leur quotidien, se conseiller, s’épauler et d’autre part pour avoir une idée de l’évolution de la maladie. Ils peuvent aussi se regrouper en associations dans le but de communiquer et de lever des fonds pour encourager les travaux de recherche dans ce domaine. Il y a sans doute d’autres patients dans le monde avec une mutation de la Neurobeachin, dont on pense simplement qu’ils sont épileptiques ou qu’ils ont un trouble du neuro-développement. Le véritable enjeu aujourd’hui est d’associer les deux, troubles du neuro-développement et Neurobeachin, pour que les généticiens testent aussi ce nouveau gène si les symptômes sont concordants.
Que sait-on sur la Neurobeachin (NBEA)?
Il existe encore peu d’informations sur cette protéine. Elle est essentiellement exprimée dans le cerveau et joue vraisemblablement un rôle très important dans les systèmes de contrôle de l’activité cérébrale. NBEA a été identifié comme gène candidat pour des maladies avec TND en 2003. Une simple mutation de ce gène peut entraîner des conséquences très sévères du point de vue neuro-développemental. Certains gènes supportent facilement des mutations dans leur séquence. D’ailleurs, si l’on compare le génome de deux personnes lambda, on va s’apercevoir qu’il y a beaucoup de différences entre elles, ce qui est tout à fait normal. Mais certains de nos gènes supportent moins bien les mutations. NBEA est un exemple de ces gènes extrêmement contraints qui ne tolèrent presque aucune mutation.
Depuis, l’équipe de Thomas a décroché un financement sur 4 ans de l’Agence Nationale de Recherche pour mieux comprendre les bases moléculaires et cellulaires du fonctionnement de la NBEA. Il collabore aussi avec Tristan Sands de l’Université de Columbia sur la validation diagnostique chez de nouveaux patients.
« Le travail de Sonia n’avait pas du tout pour finalité de résoudre l'errance diagnostique de cette petite fille. Or c’est ce qui s’est passé, l’histoire est belle et donne du sens à notre recherche. Et cela montre à quel point la recherche fondamentale est nécessaire et importante, et qu’il ne faut pas être trop contraint dans nos idées. », souligne Thomas.
En résumé
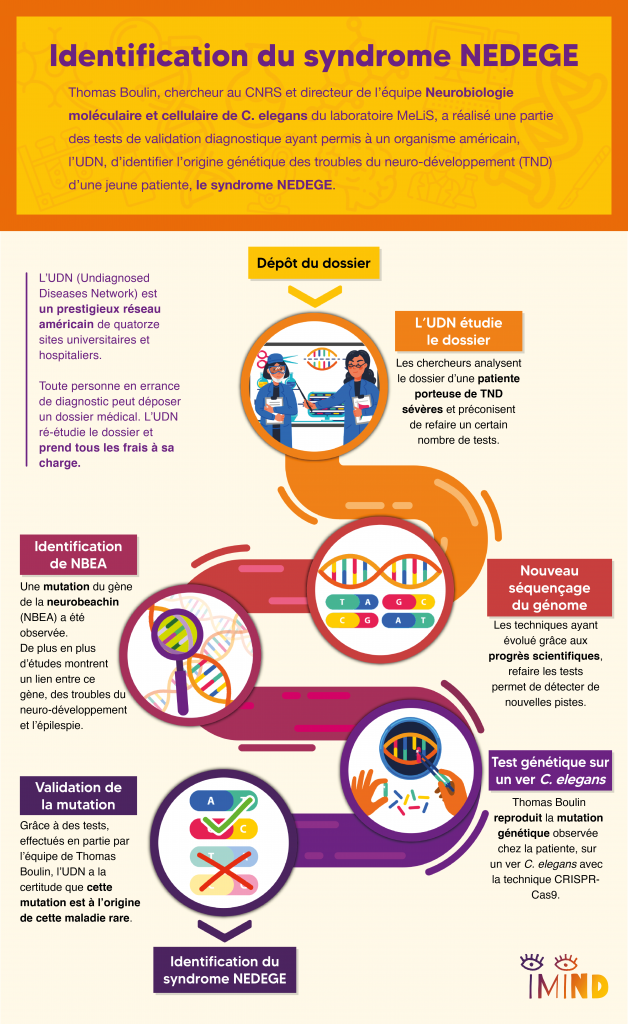

Adeline Lacroix, lauréate du Prix Jeunes Talents de l'Oréal-UNESCO 2022
Adeline Lacroix, doctorante en neurosciences au LPNC à Grenoble s’est vu remettre un Prix Jeunes Talents par l’Oréal le 12 octobre dernier. Découvrez son parcours et ses recherches!

Pouvez-vous vous présenter ?
Je suis Adeline Lacroix. J’ai 39 ans. Je suis doctorante au Laboratoire de Psychologie et NeuroCognition (LPNC) à Grenoble. J’ai commencé ma carrière professionnelle en étant professeure des écoles, puis j’ai été enseignante spécialisée en SEGPA. Je m’occupais d’élèves avec des problématiques d’apprentissage. Malgré mon intérêt pour ce travail, j’avais de plus en plus de difficultés dans mon quotidien professionnel : le bruit, la gestion de la classe, le fait de devoir faire plusieurs choses en même temps, etc… Ces difficultés ne se voyaient pas forcément de manière flagrante dans mon travail mais généraient un épuisement intense et m’ont conduit à des problèmes de santé. J’ai donc essayé de comprendre d’où cela pouvait venir. J’ai d’abord consulté une psychologue, puis je me suis rendue dans un CRA et j’ai été diagnostiquée avec un TSA. Suite à cela, je me suis beaucoup documentée sur la question, j’étais aussi très intéressée par la recherche. Ma reconversion professionnelle étant une nécessité, c’est donc tout naturellement que j’ai décidé de reprendre mes études en 2014 et je suis actuellement en fin de thèse de neurosciences.
Sur quoi porte vos recherches ?
Je travaille sur la perception visuelle des visages chez les adultes autistes. Je m’appuie sur un modèle suggérant que le traitement visuel des sujets typiques se baserait d’abord sur des caractéristiques globales, grossières des stimuli (visages ou autre). Ces informations grossières seraient envoyées dans les aires frontales pour réaliser des prédictions qui seraient réinjectées ensuite dans les aires de la reconnaissance visuelle pour favoriser une reconnaissance rapide. Or, les personnes autistes ont un traitement visuel de l’information qui est davantage axé sur les caractéristiques locales, les détails. On sait que le traitement des visages peut être particulier chez les personnes autistes. Les personnes autistes ne vont pas explorer visuellement les mêmes aires ou n’auront pas le même temps de fixation sur les différentes aires du visage que des personnes non autistes. Bien souvent, il y a des difficultés de reconnaissance des émotions, mais on ne sait pas si c’est lié à des particularités perceptives, à des difficultés de compréhension sociales plus générales ou encore à une difficulté à reconnaitre ses propres émotions. Ces trois explications peuvent d’ailleurs co-exister. De mon côté, j’étudie si les difficultés qu’ont les personnes autistes dans le traitement visuel des visages pourraient être en partie liées à des particularités perceptives en lien avec des processus prédictifs atypiques.
Vous vous êtes aussi intéressée à la question du TSA au féminin.
Effectivement, je me suis intéressée particulièrement aux femmes autistes, parce que je me suis aperçue que peu de recherches portaient sur elles, les rendant moins visibles que les hommes. Je m’intéresse aussi aux différences liées au sexe et au genre, puisque c’est un sujet qui me tient à coeur et qu’il est vraiment important d’étudier si on veut rattraper le retard diagnostique dont sont sujettes les femmes. Heureusement, beaucoup de recherches sur ce sujet se sont développées ces dernières années.
Vous êtes à l’Université de Melbourne, en Australie, pour quelques mois, dans quel but ?
J’utilise plusieurs méthodes dans mes recherches. J’étudie la réponse comportementale des personnes autistes en enregistrant leurs réponses et leur temps de réactions lors d’expériences. J’étudie également l’activité électrique de leur cerveau avec l’électroencéphalographie (EEG) ce qui me permet de mesurer l’amplitude et la latence de leur réponse cérébrale lors du traitement des visages. L’EEG est très précis d’un point de vue temporel mais moins d’un point de vue spatial. Pour connaitre les aires impliquées dans la réponse observée, nous avons des techniques pour reconstituer les sources. Au degré encore supérieur, il existe une technique, la DCM (Dynamic Causal Modeling), qui permet d’étudier la connectivité effective entre les aires. Cela permet de comprendre l’influence d’une aire sur une autre lors d’un traitement. Je suis venue à Melbourne pour apprendre cette technique au sein de l’équipe de Marta Garrido, qui a fait sa thèse et qui collabore avec Karl Friston, à l’origine du DCM (Dynamic Causal Modeling).
Qu’avez-vous prévu pour la suite ?
Dans un premier temps, je vais finir ma mobilité à Melbourne puis rentrer en France pour soutenir ma thèse. Ensuite, je vais rejoindre l’équipe iMIND pour quelques mois pour avancer sur le projet autisme et parentalité. Puis, je vais retourner au LPNC pour faire un post-doc. Dans un futur plus ou moins proche, j’aimerais avoir un poste dans la recherche. Mais je sais que c’est difficile. Donc on verra…

L'hormone GnRH améliore-t-elle les fonctions cognitives des personnes porteuses de trisomie 21 ?
La récente publication de travaux dans la revue Science le 2 Septembre 2022 portant sur l’utilisation d’hormones GnRH pour améliorer les fonctions cognitives des personnes porteuses de trisomie 21, a suscité de nombreuses réactions au sein de la communauté scientifique. Nous sommes allés à la rencontre du Professeur Damien Sanlaville, chef du Service de Génétique aux Hospices Civils de Lyon, afin qu’il nous livre plus de précisions sur ces résultats.

Une étude internationale
L’équipe du Centre Hospitalier Universitaire Vaudois (CHUV, Lausanne), Lausanne, Suisse ont collaboré avec une équipe de l’INSERM au sein du laboratoire Lille neuroscience & cognition afin de tester l’efficacité d’une thérapie fondée sur l’injection de l’hormone GnRH, pour améliorer les fonctions cognitives d’un petit groupe de patients porteurs de trisomie 21. Ils ont publié leurs résultats dans la prestigieuse revue scientifique Science le 2 septembre 2022.
Premières observations
Les scientifiques ont d’abord mis en évidence un dysfonctionnement des neurones récepteurs à la GnRH dans un modèle animal de trisomie 21 et étudié ses conséquences sur l’altération des fonctions cognitives. Ils ont pu montrer que cinq brins de micro-ARN régulant la production de cette hormone et présents sur le chromosome 21 étaient dérégulés. Ensuite, ils sont parvenus à démontrer sur un modèle de souris que les déficiences cognitives et olfactives étaient étroitement liées à une sécrétion dysfonctionnelle de GnRH. Ils ont également pu démontrer que la remise en fonction d’un système GnRH physiologique permettait de restaurer en partie, au bout de 15 jours, les fonctions cognitives et olfactives chez la souris trisomique.
Des résultats prometteurs…
Suite à ces résultats très encourageants, une étude pilote a été menée chez sept hommes, adultes, âgés de 20 à 50 ans, porteurs de trisomie 21 pour tester une thérapie basée sur l’injection pulsatile de GnRH avec pour objectif une amélioration des fonctions cognitives et de la connectivité cérébrale. Ils ont reçu une dose de GnRH toutes les deux heures en sous-cutané pendant 6 mois, à l’aide d’une pompe placée sur le bras. Des tests de la cognition et de l’odorat ainsi que des examens IRM ont été réalisés avant et après le traitement.
D’un point de vue clinique, les performances cognitives ont augmenté chez 6 des 7 patients, chez qui on observe une meilleure représentation tridimensionnelle, une meilleure compréhension des consignes, une amélioration du raisonnement, de l’attention et de la mémoire épisodique. En revanche, le traitement n’a pas eu d’impact sur l’olfaction. Aucun effet indésirable notable n’a été rapporté.
… qui restent à confirmer
La communauté scientifique et médicale se réjouit de tels résultats, mais nous devons rappeler que de nombreux médicaments se sont révélés prometteurs chez les souris trisomiques, mais, à ce jour, aucun n’a fonctionné de façon probante lors des essais sur l’Homme. De plus l’effet placebo est important, en particulier chez les patients avec trouble du développement intellectuel. Ainsi, il est nécessaire de faire une étude clinique plus importante en double aveugle, permettant de mieux mesurer l’effet réel de ce traitement. Il faudra également être attentif aux échelles d’évaluation qui seront utilisées.
Par ce court article, nous soulignons cette avancée, mais nous ne souhaitons pas donner de faux espoir aux personnes porteuses de trisomie 21 et de leurs familles. Attendons donc les résultats de l’étude clinique qui, nous l’espérons, sera rapidement réalisée.
Article rédigé par le Pr Damien Sanlaville.
Ressources:
- GnRH replacement rescues cognition in Down syndrome : Pour consulter l’article en question sur Science
- Trisomie 21 France – Pour plus d’informations sur la trisomie 21
- Communiqué de presse INSERM
- Journée mondiale de la Trisomie 21 avec Damien Sanlaville et Michel Till
Clinique
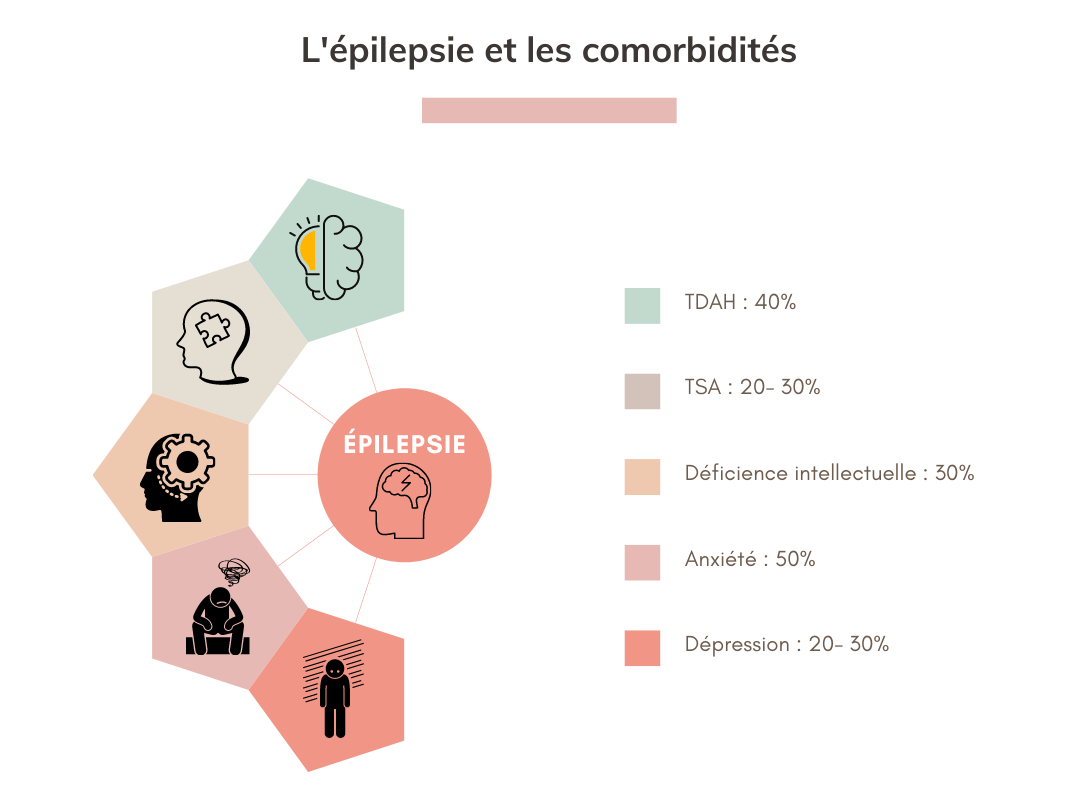
A lire également
L’épilepsie et les troubles du neurodéveloppement : quel est le lien ?
Françoise THOMAS-VIALETTES, vice-présidente EPI et expert EFAPPE, explique pourquoi il est important de comprendre les liens entre l’épilepsie et les TND.
En savoir plus
Les neurotransmetteurs : notions de base
Que sont les neurotransmetteurs ?
Les neurotransmetteurs sont les messagers chimiques de votre corps. Ils transmettent des messages d’une cellule nerveuse à une autre cellule cible, qui peut être une cellule nerveuse, musculaire ou glandulaire. Actuellement les scientifiques connaissent l’existence d’au moins 100 neurotransmetteurs et soupçonnent qu’il en existe beaucoup plus.
Le corps possède un vaste réseau de nerfs (le système nerveux) qui envoie et reçoit des signaux électriques entre les cellules nerveuses et leurs cellules cibles dans tout le corps.
Le système nerveux contrôle tout, de votre esprit à vos muscles, ainsi que les fonctions de vos organes. En d’autres termes, les nerfs sont impliqués dans tout ce que vous faites, pensez et ressentez. Les cellules nerveuses envoient et reçoivent des informations de toutes les parties du corps. Cette ‘feedback’ constante est essentielle au fonctionnement optimal de votre corps.
Quelles fonctions corporelles les nerfs et les neurotransmetteurs aident-ils à contrôler ?
Votre système nerveux contrôle des fonctions telles que :
- Le rythme cardiaque et la pression sanguine.
- La respiration.
- Les mouvements musculaires.
- Pensées, mémoire, apprentissage et sentiments.
- Le sommeil, la guérison et le vieillissement.
- La réponse au stress.
- La régulation hormonale.
- La digestion, la sensation de faim et de soif.
- Les sens (réponse à ce que l’on voit, entend, sent, touche et goûte).
Où se trouvent les neurotransmetteurs ?
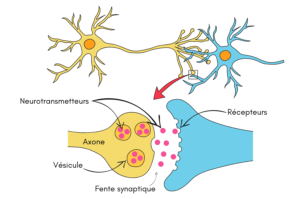
Nous avons des milliards de cellules nerveuses dans notre corps. Les cellules nerveuses sont généralement constituées de trois parties :
Vésicules synaptiques sont de petits compartiments des terminaux présynaptiques des neurones, stockant des neurotransmetteurs qui sont susceptibles d’être libérés dans l’espace intersynaptique.
Un axone. L’axone transporte les signaux électriques le long de la cellule nerveuse jusqu’au terminal de l’axone.
Un terminal de l’axone. C’est là que le message électrique est transformé en signal chimique à l’aide de neurotransmetteurs pour communiquer avec le groupe suivant de cellules nerveuses, de cellules musculaires ou d’organes. Les neurotransmetteurs sont situés dans cette partie.
Les actions des neurotransmetteurs
Les neurotransmetteurs transmettent une des trois actions possibles dans leurs ‘messages’, selon le neurotransmetteur spécifique.
Excitateur : Les neurotransmetteurs excitateurs « excitent » le neurone et lui font « envoyer le message », c’est-à-dire que le message continue à être transmis à la cellule suivante. Le glutamate, l’épinéphrine et la norépinéphrine sont des exemples de neurotransmetteurs excitateurs.
Inhibiteurs : Les neurotransmetteurs inhibiteurs bloquent ou empêchent le message chimique d’être transmis plus loin. L’acide gamma-aminobutyrique (GABA), la glycine et la sérotonine sont des exemples de neurotransmetteurs inhibiteurs.
Modulateurs : Les neurotransmetteurs modulateurs influencent les effets des autres messagers chimiques. Ils « tordent » ou ajustent la façon dont les cellules communiquent au niveau de la synapse. Ils affectent également un plus grand nombre de neurones en même temps.
Une fois que les neurotransmetteurs ont transmis leur message, soit ils se dissipent, soit ils sont réabsorbés et réutilisés par la cellule qui les a émis, soit ils sont décomposés par des enzymes dans la synapse.

Sondage sur les préférences des personnes neuroatypiques concernant les espaces publics
Tout le monde devrait pouvoir profiter des espaces publics, mais ceux-ci ne sont pas toujours adaptés aux besoins des personnes neuroatypiques. Nous menons une étude préliminaire avec un groupe de travail du pôle HU-ADIS au Centre Hospitalier Le Vinatier et des personnes concernées, pour mieux comprendre les freins qui empêchent les individus de profiter pleinement des espaces publics.
Si vous êtes porteurs d’un TSA, TDAH, troubles DYS, … aidez-vous à améliorer votre accueil dans l’espace urbain !

Newsletter

Quoi de neuf chez SIBIUS?
Créée à Lyon en 2019 à la suite d’un transfert de technologie d’une invention brevetée du CNRS opéré par PULSALYS, la startup SIBIUS développe une plate-forme basée sur l’intelligence artificielle destinée à améliorer la détection et le suivi des troubles cognitifs. Utilisant le support d’une simple tablette, la solution de SIBIUS mesure l’attention visuelle grâce à l’exploration tactile d’images.

Premiers résultats concluants pour Digitrack
En effet, grâce à un partenariat avec la métropole de Lyon via les PMI, 115 enfants en école maternelle, âgés de 3 et 4 en majorité, ont été testés de façon systématique et les résultats sont très concluants. Parmi eux, vingt-trois enfants présentaient un profil atypique. Dix d’entre eux étaient suivis pour des troubles déjà identifiés, marquant ainsi la robustesse du test DIGITRACK. Les treize autres enfants, sans symptôme particulier, présentaient des profils potentiellement à risque de trouble du spectre de l’autisme, trouble de l’attention, ou encore déficience intellectuelle. Grâce à cela, les médecins de la PMI ont pu communiquer avec les familles pour mettre en place un suivi adéquat. Il est aussi envisagé de développer une détection systématique à un autre moment charnière : l’entrée au CP. Une discussion avec le Ville de Lyon va s’ouvrir à ce sujet.
Dépister en priorité les enfants nés prématurés…
Grâce au soutien financier de la Région Auvergne Rhône-Alpes, SIBIUS a lancé une expérimentation auprès de plusieurs services de néonatalogie (Lyon, Saint-Etienne, Grenoble, Clermont-Ferrand) afin de tester systématiquement les enfants nés prématurément. Cette population est en effet 70% plus susceptible de développer des troubles du neurodéveloppement. Un dépistage précoce permet ainsi un suivi au plus près des besoins de chaque enfant. L’expérimentation devrait commencer dès la rentrée de septembre. Les enfants concernés ayant des consultations régulières jusqu’à l’âge de 7 ans, le dépistage DIGITRACK sera intégré au cours de ce suivi.
… et les personnes vieillissantes
La collecte de données a démarré auprès de cette population pour pouvoir détecter des troubles de type Alzheimer et démence au plus tôt. Ce travail en phase de R&D a un objectif ambitieux, mieux comprendre et modéliser l’évolution des fonctions cognitives à travers les âges, permettant ainsi d’élaborer des trajectoires cognitives et d’identifier les variables qui les influencent.
Commercialisation d’un premier produit d’ici la fin de l’année
Une levée de fonds est en cours dans l’objectif de commercialiser une solution digitale pour aider les médecins de ville à la détection précoce de troubles du neurodéveloppement auprès de leur jeune patientèle. Il devrait être disponible prochainement sur différents réseaux de distribution. Affaire à suivre…
Ressources:
- Communiqué de presse SIBIUS – 2 avril 2022
- Site internet SIBIUS
Newsletter

À la découverte des cinq centres d'excellence
Venez découvrir les cinq centres d’excellence au travers de courtes vidéos présentant des projets impactants pour les personnes concernées!
Dans le cadre de la stratégie nationale 2018-2022, le Secrétariat d’état chargé des personnes handicapées lançait un appel à projets visant à identifier des centres permettant de créer un réseau de recherche d’excellence sur l’autisme et les troubles du neuro-développement.
Cet appel à projets a permis l’identification des centres d’excellence CeAND (Montpellier), Exac-T (Tours) et INOVAND (Paris) en 2019, suivis des pôles iMIND (Lyon) et STRAS&ND (Strasbourg) à l’issue d’une seconde phase de labellisation lancée en 2020.
La création de ces centres d’excellence répond à plusieurs objectifs : établir un continuum entre l’expertise diagnostique et thérapeutique, la recherche clinique et fondamentale ainsi que la formation universitaire.
Zoom sur des projets de recherche
Nous vous proposons de découvrir ces 5 centres d’excellence au cours de la semaine du 04 au 08 avril 2022. Chaque centre diffusera, au travers de vidéos, des projets de recherche translationnelle au bénéfice des personnes concernées.
Pour cela les centres d’excellence vous donnent RDV chaque jour à 12h00 sur leurs réseaux sociaux et sites internet afin de découvrir leurs travaux.
CeAND – Lundi 4/04
Le CeAND présente ENVIRODISORDERS, un projet multidisciplinaire proposant une approche à la fois clinique et expérimentale pour comprendre le rôle de la génétique et des contaminants environnementaux, tels que le glyphosate, dans le développement des Troubles du Spectre Autistique (TSA).
iMIND – Mardi 5/04
Un projet co-porté par le Centre hospitalier le Vinatier, l’institut Marc Jeannerod et le centre iMIND est en cours pour déterminer, selon des critères neuroscientifiques, les leviers de bien-être de personnes autistes dans des espaces architecturaux.
Stras&ND – Mercredi 6/04
InovAND – Jeudi 7/04
Exac.T – Vendredi 8/04
Le Centre d’Excellence sur l’Autisme et les Troubles du Neurodéveloppement Exac·t présente l’étude SEVIRE (Sensory Virtual Reality, CHRU de Tours), projet utilisant la réalité immersive pour entrainer les capacités de traitement multisensoriel d’enfants avec un Trouble du Spectre de l’Autisme.
Newsletter

Laurie-Anne Sapey Triomphe récompensée pour ses travaux sur l'autisme
La Métropole de Lyon et la Ville de Lyon en partenariat avec l’Université de Lyon, ont décerné le Prix de la Jeune Recherche 2021. Trois chercheurs ont été récompensés dont Laurie-Anne Sapey Triomphe, ancienne doctorante du CRNL, qui travaille sur l’autisme.
Pouvez-vous vous présenter?
Je suis Laurie-Anne Sapey-Triomphe. Je suis actuellement chercheuse post-doctorante à KU Leuven en Belgique. J’ai commencé par étudier la biologie à l’ENS de Lyon où j’ai fait un master recherche et un master enseignement. J’ai ensuite continué avec un doctorat de neurosciences au CRNL sous la direction de Christina Schmitz et Jérémie Mattout. Mes travaux de thèse portaient sur la perception chez les adultes autistes. Puis, je suis partie en post-doc en Belgique au sein du laboratoire de Johan Wagemans qui a élaboré les théories sur lesquelles j’ai basé ma thèse : essayer de comprendre l’autisme par le prisme de la théorie du cerveau prédictif ou cerveau bayésien.
Vous avez reçu un prix de la Métropole de Lyon pour vos travaux sur l’autisme, pouvez-vous nous en dire plus ?
J’étudie la perception, surtout visuelle et tactile chez les adultes autistes. Selon la théorie du cerveau prédictif, pour nous aider à traiter la quantité de stimuli auxquels nous sommes confrontés chaque jour, notre cerveau se construit des représentations internes au fil du temps, qui l’aide à simplifier et à traiter les informations plus efficacement et rapidement. Les informations reçues par notre cerveau sont comparées à ces représentations ou a priori. Notre perception résulte donc du mélange entre l’information sensorielle réelle et nos a priori. Cette théorie s’est révélée particulièrement intéressante dans le cadre de l’autisme car elle permettait d’expliquer l’hétérogénéité des particularités autistiques. Au départ, on pensait que les personnes autistes ne pouvaient pas se construire d’a priori ce qui rendait leur environnement imprédictible et donc plus difficile à appréhender. En effet, pour évoluer dans un monde avec énormément d’information à traiter en même temps, il faut être capable de filtrer les informations non pertinentes, ce qui est très difficile si on n’a pas ces a priori pour nous aider. Les intérêts restreints et les comportements répétitifs étaient perçus comme un moyen de restaurer une certaine forme de prédictibilité.
Cette théorie a finalement dû être nuancée car certaines expériences relatées dans la littérature scientifique ont montré que les personnes autistes peuvent se former des a priori, mais qui sont parfois tellement précis qu’ils n’aideraient pas au processus de synthétisation de l’information. En effet, si on compare l’information nouvelle avec un a priori très précis, il risque d’y avoir peu de superposition et cela ne va pas aider à simplifier la compréhension.
Nous avons aussi pu observer des choses intéressantes sur la dynamique d’ajustement de ces a priori. Quand ces a priori sont construits dans un certain contexte, mais qu’au fur et à mesure, cette règle devient de moins en moins fiable, alors on va ajuster notre a priori pour être un peu plus flexible. Chez les personnes autistes, cette dynamique d’ajustement serait moins rapide. Si elles se sont construites un a priori très fort, alors ce serait plus difficile de le redéfinir ou de l’ajuster, ce qui expliquerait qu’elles ont plus de difficultés à tolérer les changements, les incertitudes.
Quels outils utilisez-vous pour mettre tout cela en évidence ?
On étudie les comportements de groupes de personnes autistes et de groupes de personnes qu’on appelle « contrôle ». Mais je suis aussi très intéressée de voir ce qui se passe au niveau cérébral et moléculaire pour avoir une sorte de continuum entre le comportement, le fonctionnement cérébral et les corrélats moléculaires.
On utilise par exemple la spectroscopie par résonnance magnétique pour mesurer la concentration de certains neurotransmetteurs. Nous avons donc mesuré les deux neurotransmetteurs principaux qui agissent dans le gyrus frontal inférieur droit qui est une région impliquée dans l’apprentissage des a priori. Il s’agit du glutamate, un neurotransmetteur excitateur qui facilite le passage de l’information, et du gaba, un neurotransmetteur inhibiteur qui, à l’inverse, réduit la quantité d’information transmise. On a observé que les ratios glutamate/gaba étaient corrélés à la capacité d’apprentissage des a priori, et que les personnes autistes avaient plus de glutamate dans cette région que les contrôles. Cela signifie qu’il y a plus d’information qui passe, mais potentiellement plus parasitée. Pour l’instant, cela reste juste des corrélations, mais ce sont des pistes pour essayer de mieux comprendre les bases moléculaires de l’autisme.
Vous êtes de retour à Lyon, des projets ?
Mon post-doc en Belgique se termine fin août, et j’ai quelques pistes auprès d’équipes lyonnaises pour la suite, mais nous sommes en attente de réponse des demandes de financement. L’année prochaine, je compte préparer les concours de chercheurs CNRS et Inserm et d’enseignant-chercheur. Mais d’ici là, j’ai quelques projets à finaliser à Leuven, notamment un projet pour comprendre comment faciliter l’apprentissage des enfants autistes. Nous sommes en train de tester dans quel contexte les jeunes enfants autistes vont plus facilement pouvoir se créer des a priori : serait-ce dans un environnement très variable avec tout l’éventail des possibles pour qu’ils se créent très tôt des a priori ou, au contraire, est-ce qu’il faut amener la variabilité petit à petit pour leur permettre d’ajuster à leur rythme… La question reste entière !
Newsletter
Étude PrémiCeS22
Appel à participation à l’étude des réponses comportementales associées au traitement de l’information faciale émotionnelle chez les enfants porteurs d’une délétion 22q11.2
Promoteur : CH Le Vinatier
Investigateur : Mme Marie-Noëlle BABINET
Contact : marie-noelle.babinet@ch-le-vinatier.fr

Objectifs de la recherche
Nous souhaitons mieux comprendre les réponses comportementales associées au traitement de l’information faciale émo-tionnelle chez les enfants porteurs d’une délétion 22q11.2.
Pour cela, nous allons essayer de :
(i) Mieux caractériser les compétences et les fragilités des enfants (4-13 ans) por-teurs d’une délétion 22 dans le domaine des aspects émotionnels de la cognition sociale.
(ii) Déterminer si ces difficultés sont sous-tendues par des processus attentionnels et/ou visuo-spatiaux.
(iii) Déterminer si les difficultés comporte-mentales rapportées par les familles de ces enfants sont sous-tendues par des difficul-tés spécifiques dans la reconnaissance des émotions faciales, le traitement de la direc-tion du regard d’autrui et par un traite-ment perceptif atypique des visages.
Contexte
La délétion 22q11.2 est l’un des syndromes de microdélétion les plus fréquents (1/2000-1/4000 naissances) et l’un des facteurs de risque génétique les plus robustes de la schi-zophrénie (1 à 2% de délétion 22q11.2 chez les personnes atteintes de schizophrénie).
Les enfants porteurs d’une délétion 22q11.2 présentent souvent des compétences sociales plus faibles que les jeunes au développement typique. Ces difficultés d’adaptation aux si-tuations sociales et aux relations interperson-nelles pourraient être sous-tendues par des altérations des processus cognitifs sociaux et pourraient également être liés à l’émergence de signes psychotiques.
Intérêt clinique de la recherche
La question d’une meilleure compréhen-sion des signes précurseurs à l’émergence de signes psychotiques est un enjeu ma-jeur dans la prise en charge de ces enfants et adolescents.
De plus, la question de l’origine des pro-cessus cognitifs sociaux reste à ce jour peu explorée.
Qui peut participer ?
- des enfants âgés de 4 à 13 ans porteurs de la délétion 22q11.2
- des enfants âgés de 4 à 13 ans qui n’ont pas de trouble du neurodéveloppement
Déroulé de la recherche
1. Evaluation pour connaitre le niveau global de l’enfant si cela n’a pas déjà été réalisé
2. Passation de trois tâches expérimentales évaluant les aspects émotionnels de la cognition sociale
3. Evaluation des processus cognitifs attentionnels et visuospatiaux
4. Passation de trois tâches com-portementales simples sur ordinateur
Une fois l’étude terminée, l’enfant et ses parents recevront un compte-rendu dé-taillé des différentes évaluations.
Infos pratiques
Lieu:
GénoPsy – Centre de Référence Maladies Rares à Expression Psychiatrique
Centre Hospitalier le Vinatier
95 Bd Pinel, 69500 BRON
Bâtiment 505, RDC
Pour participer ou poser vos questions, contactez :
Mme Marie-Noëlle BABINET
Newsletter
Nouvelle recherche : Differential fate between oxytocin and vasopressin cells in the developing mouse brain
Eclairer notre compréhension de l’autisme avec la transparisation et l’imagerie cellulaire en 3 dimensions.
Nouvelles recherches !
Une équipe de recherche hybride Vinatier/ISC Marc Jeannerod (Amélie Soumier, Marie Habart, Guillaume Lio, Caroline Demily & Angela Sirigu) au sein d’iMIND, a trouvé que les neurones qui fabriquent l’ocytocine, contre toute attente, continuent de se développer après la naissance. L’ocytocine, dite ‘l’hormone de l’amour’, est importante dans la création du lien social, et présente un potentiel thérapeutique pour les personnes sur le spectre de l’autisme.
Par contre, ce phénomène de développement post-natal ne touche pas les neurones de la Vasopressine, qui sont très proches en terme de fonction et de structure.
Ils pensent donc qu’il existe plusieurs réseaux de l’ocytocine qui pourraient être impliqués différemment dans le développement des troubles sociaux notamment. Il existerait un réseau « inné » qui est présent à la naissance, et un réseau qui se développe après la naissance, dit « adaptatif », qui pourrait dépendre de nos expériences sociales.
Cette découverte va nous permettre à terme d’accélérer la recherche thérapeutique, et de pouvoir tester plus rapidement l’efficacité de différents médicaments.


